Воспламенение и горение – важнейшие стадии физико-химических превращений горючего и окислителя в любых рабочих процессах двигателей внутреннего сгорания. Несмотря на большие достижения в области теории горения вообще и теории рабочих процессов в частности, а также несмотря на непрерывное конструктивное совершенствование современных двигателей, полезная теплота составляет 30-40 % теплоты, выделяющейся при горении различных видов топлива.
Дальнейшее совершенствование двигателей внутреннего сгорания в значительной мере зависит от возможности регулирования отдельных стадий процессов воспламенения и горения и обеспечения эффективного их протекания и недопущения различных отклонений, вызывающих ухудшение мощностных и экономических показателей работы двигателей.
Общая характеристика процессов воспламенения и горения
Для понимания особенностей рабочих процессов в двигателях различного типа, обоснования требований к качеству горючего, а также для правильного решения ряда практических вопросов его применения, хранения и транспортировки необходимо знать общие закономерности и условия осуществления процессов воспламенения и горения. Это имеет большое значение также для обеспечения безопасности обращения с горючим, исключения возможностей возникновения пожаров и взрывов.
Горение – сложный комплекс физико-химических превращений смеси горючего и окислителя, сопровождающийся интенсивным выделением теплоты и излучением света. В основе процесса горения лежит химическая реакция, развивающаяся в условиях прогрессивного самоускорения, связанного с накоплением в системе теплоты и катализирующих процесс промежуточных продуктов реакции. Несмотря на то что в основе горения лежат химические превращения горючего и окислителя, развитие процесса определяется наряду с химической кинетикой физическими процессами (распыливанием, испарением, смешением горючего и окислителя) и условиями передачи теплоты и вещества из зоны реакции в свежую горючую смесь. Наиболее общей и специфической чертой процесса горения является резкое экспоненциальное ускорение химической реакции при выделении теплоты самой реакции и образовании активных продуктов, приводящее к прогрессивному саморазгону.
Физико-химические превращения, в результате которых становится возможным быстрое прогрессивное протекание химической реакции, можно рассматривать как самостоятельный суммарный процесс, который называют воспламенением.
Воспламенение всегда предшествует процессу горения, представляемому как процесс распространения зоны быстрой химической реакции по исходной горючей смеси, и тесно связано с ним. Сложные физико-химические превращения горючего и окислителя в этих процессах включают отдельные характерные стадии, на которые можно воздействовать, изменяя условия их развития. В зависимости от свойств горючей смеси и условий воспламенения и горения могут значительно меняться как физическая картина процессов, так и механизм воспламенения и распространения зоны реакции.
Учитывая условия подачи горючего и окислителя в зону реакций и их фазовое состояние, можно выделить две группы процессов:
- воспламенение и горение газообразных горючих смесей;
- горение распыленного жидкого горючего.
Каждая группа процессов в свою очередь может протекать в диффузионной и кинетической областях.
Процессы в диффузионной области осуществляются тогда, когда суммарная скорость физико-химических превращений (количество горючей смеси, сгорающей в единицу времени, отнесенное к единице объема камеры сгорания или поверхности фронта пламени) зависит главным образом от скорости смещения горючих и окислительных компонентов. Это явление наблюдается при раздельной подаче горючего и окислителя и при таких условиях, когда химические превращения протекают со столь значительной скоростью, что в общей последовательности всех стадий процессов воспламенения и горения главным тормозящим фактором становятся физические процессы подготовки горючей смеси.
В диффузионной области решающую роль играют гидродинамические факторы и меньшее влияние оказывают свойства горючего и окислителя.
В кинетической области общая скорость физико-химических превращений в основном зависит от химических превращений и особенно велика роль свойств воспламеняемости и горючести реагирующей смеси. В этой области наряду с химическими процессами имеют значение и физические процессы передачи теплоты и продуктов реакции из зоны реакции в свежую смесь.
Для заданной горючей смеси, в зависимости от условий, процессы воспламенения и горения могут переходить из одной области в другую. С точки зрения устойчивости и возможности регулирования кинетическая область воспламенения и горения менее выгодна, так как она сохраняется в более узком диапазоне изменений условий протекания процессов, чем диффузионная.
Известны вполне определенные условия не только перехода процессов воспламенения и горения из одной области в другую, но и вообще возможности осуществления этих процессов. Процессы воспламенения и горения могут происходить при соблюдении определенных условий, которые включают следующее:
- паро- или газообразное состояние компонентов горючего и окислителя;
- определенное соотношение горючих и окислительных компонентов в паровой или газовой фазе, обусловливающее концентрационные пределы воспламенения и распространения зоны горения, вне которых эти процессы не развиваются;
- возможность накопления в реагирующей горючей смеси теплоты и активных промежуточных продуктов в количестве, обеспечивающем прогрессивное самоускорение реакции.
Паро- или газообразное состояние компонентов горючего и окислителя является необходимым условием воспламенения и последующего распространения зоны горения. Отдельные стадии предпламенных физико-химических превращений развиваются и в жидкой фазе компонентов. Образующиеся в этих процессах продукты могут существенно влиять на последующие стадии процессов воспламенения и горения. Однако прогрессивное самоускорение химической реакции, завершающееся возникновением очагов горения и их распространением по горючей смеси, возможно только в паровой фазе.
Различают верхний (высший) и нижний (низший) пределы воспламенения.
Они соответствуют таким концентрациям горючего в смеси с окислителем, при которых повышение содержания горючего (верхний предел) или уменьшение содержания горючего (нижний предел) не вызывает воспламенения и распространения зоны горения. В сильно разбавленной окислителем или чрезмерно богатой горючим смеси воспламенение не возникает, химические реакции развиваются медленно, активных промежуточных продуктов образуется недостаточно для быстрого развития процесса, а отвод теплоты при энергетическом обмене с внешней средой превышает тепловыделение в ходе реакции. Если в какой-то части смеси воспламенение и осуществится, то вследствие очень малой скорости распространения пламя в таких смесях затухает.
Существуют также пределы по давлению, вне которых в смеси заданного состава при определенной температуре не может наступить воспламенение.
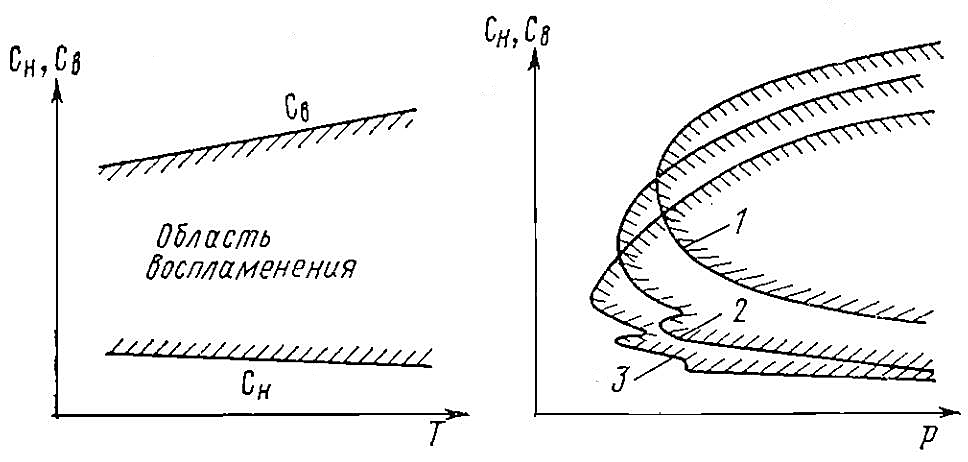
Зависимости между критическими значениями температуры и давления, при которых возможно воспламенение, приведены на рис. 1.
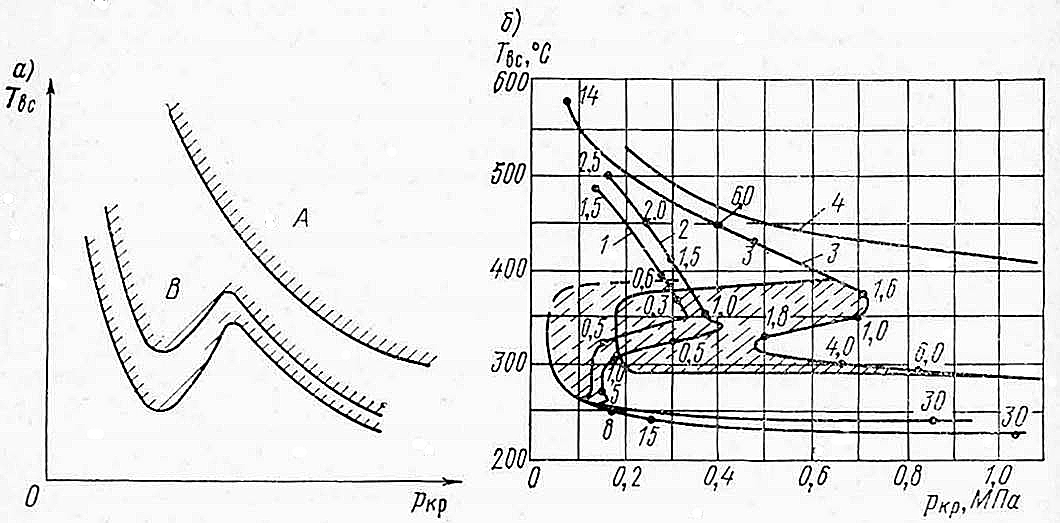
а – области:
А – теплового воспламенения; В – цепного воспламенения;
б – зависимости Tвс = f (pкр) для углеводородов.
1 – н-октан; 2 – н-гептан; 3 – изо-октан; 4 – этилен. Цифры на кривых показывают задержку воспламенения, с
Как правило, при высоких давлениях критические значения этих параметров соответствуют кривой A (рис. 1, а).
Механизм воспламенения и горения
Воспламенение связано с накоплением в реагирующей смеси теплоты и активных промежуточных продуктов в количестве, обеспечивающем прогрессивное самоускорение реакции. Если скорость выделения теплоты в ходе химических превращений превысит скорость отвода теплоты в окружающую среду с учетом всех форм энергетического обмена с ней или если скорость зарождения активных частиц реакции превысит скорость их гибели, то при определенном значении температуры или концентрации активных частиц дальнейшее прогрессивное самоускорение реакции вызывает воспламенение.
В зависимости от того, какие причины приводят к прогрессивному самоускорению реакции в процессе воспламенения (накопление в системе теплоты или активных продуктов), возможно тепловое или цепное воспламенение.
Сущность теплового воспламенения заключается в следующем.
При взаимодействии реагирующей смеси с внешней средой соотношение между количеством теплоты, выделяющейся в ходе реакции Qx. p, и количеством теплоты QΣ, затрачиваемой на различные виды энергетического обмена:
- нагревание горючей смеси;
- испарение;
- внешнюю работу;
- отвод теплоты в стенки реакционного сосуда и т. д.;
может быть как благоприятным, так и неблагоприятным для развития химических реакций.
Если скорость выделения теплоты в ходе химических превращений dQx. p/dτ превысит скорость отвода теплоты dQΣ/dτ при энергетическом обмене с внешней средой, начинается прогрессирующий разогрев горючей смеси, приводящий к самопроизвольному возрастанию скорости реакций и практически мгновенному выделению теплоты и появлению пламени.
Скорость выделения теплоты в ходе химических реакций в условиях теплового воспламенения:
где:
- wx. p – скорость химических реакций;
- E – энергия активации;
- R – газовая постоянная;
- T – температура.
Критическим пределом теплового взрыва являются либо температура самовоспламенения Tвс, выше которой при постоянном давлении возникает взрыв, либо давление pкр, выше которого при постоянной температуре осуществляется воспламенение. Зависимость между критическим давлением теплового взрыва pкр, начальной температурой T0 и энергией активации E имеет вид:
Сущность цепного воспламенения заключается в следующем.
Химические превращения при воспламенении и горении являются сложными. В таких реакциях превращение исходных веществ в конечные продукты протекает с образованием ряда промежуточных соединений. Значительную роль при этом играют активные частицы, легко вступающие в реакции с исходными или промежуточными продуктами. Активными частицами чаще всего бывают монорадикалы, например:
- RCH2—,
- HO—,
- HOO—,
и реже бирадикалы:
- —O—,
- —CH2— и др.
Для горючих смесей, реагирующих по цепному механизму, образование активных промежуточных продуктов ускоряет химическую реакцию. Изменение концентрации активных продуктов со временем происходит по уравнению:
где:
- kз. ц, kр. ц, kо. ц – кинетические константы, характеризующие соответственно скорость зарождения цепей, скорость процесса разветвления и скорость процесса обрыва цепей.
Стационарный режим протекания реакций возможен, если kо. ц > kр. з. Тогда концентрация активных продуктов с течением времени стремится к квази-стационарному значению:
Скорость реакций:
Нестационарный режим протекания реакции соответствует условию kр. ц > kо. ц.
Тогда:
В соответствии с этим и скорость реакций возрастает со временем по экспоненциальному закону:
где:
- φ = kр. ц – kо. ц.
При нестационарном развитии цепных реакций резкое лавинообразное увеличение концентрации активных промежуточных продуктов приведет к такому возрастанию скорости реакции и ее самоускорению, что произойдет воспламенение.
Воспламенение называется цепочно-тепловым, если медленно развивающаяся цепная реакция самоускоряется сначала вследствие увеличения концентрации активных продуктов, а затем вследствие выделяющейся теплоты.
Как правило, все виды воспламенения протекают по цепочно-тепловому механизму, в той или иной степени приближаясь к цепному или тепловому механизму.
Цепные реакции могут развиваться достаточно медленно и исходные продукты успевают израсходоваться настолько, что скорость реакций снижается, не достигая величины, при которой начинается самоускорение и последующее воспламенение. Такое замедленное развитие цепного процесса Н. Н. Семенов назвал «вырожденным взрывом». Медленное протекание цепных реакций наблюдается, например, в случае, когда разветвление цепей осуществляется в результате распада относительно устойчивых промежуточных продуктов. При их распаде или других превращениях образуются свободные радикалы.
Если в ходе сложных реакций меняется механизм превращений, различными оказываются и температурные зависимости скорости процесса. В определенном температурном интервале скорость цепных реакций с ростом температуры может не увеличиваться при ухудшении условий образования активных центров. Это явление получило название отрицательного температурного коэффициента.
В результате медленно нарастающей скорости цепного процесса достигается скорость тепловыделения, превышающая скорость отвода теплоты в окружающую среду. Станут возможными прогрессивный саморазогрев смеси и дальнейшее ускорение реакций уже не за счет увеличения концентрации активных продуктов, а за счет повышения температуры.
В цепочно-тепловом воспламенении цепное ускорение реакций играет роль предварительного процесса, создающего условия для теплового воспламенения.
При относительно низкой температуре значительного числа активных центров не образуется, цепочно-тепловое воспламенение развивается медленно и протекает через ряд стадий. Например, для смесей углеводородов с кислородом воздуха возможно многостадийное воспламенение с последовательным образованием так называемого холодного и обычного горячего пламени. Образование холодного пламени обусловлено диффузией радикалов из зоны реакции в свежую смесь. Свечение холодного пламени вызывается химическим возбуждением формальдегида, образующегося в этом процессе. Механизм распространения зоны реакции в процессе горения может быть различным. Существует нормальное, или тихое, цепное, детонационное распространение зоны горения путем умножения очагов самовоспламенения (последовательное самовоспламенение объемов горючей смеси).
Как правило, процесс горения осуществляется во фронте пламени, имеющем определенные поверхность и толщину (рис. 2).

1 – зона подогрева исходной смеси от T0 до Tвс (толщина зоны δп); 2 – зона химических реакций (толщина зоны δx. р); 3 – зона продуктов сгорания
Фронт пламени отделяет область еще не прореагировавшей горючей исходной смеси от области продуктов сгорания. Даже при горении газообразных заранее перемешанных Применение горючих газов в качестве топлива в дизельных двигателяхгорючих смесей редко наблюдается сплошной фронт пламени. Чаще всего пламя состоит из многих очагов, и зона горения распространяется по горючей смеси с различными скоростями.
Причиной нормального или тихого распространения пламени является передача теплоты и активных продуктов из зоны реакции в свежую смесь. Скорость перемещения фронта пламени в направлении X, перпендикулярном к его поверхности, называется фундаментальной или нормальной скоростью распространения пламени:
Учитывая, что распространение пламени обусловлено только передачей теплоты теплопроводностью из зоны реакции в свежую смесь и ее нагреванием от начальной температуры T0 до температуры воспламенения Tвс (см. рис. 2), можно записать:
где:
- cp ср и λср – коэффициенты теплоемкости и теплопроводности среды соответственно;
- – средний градиент температуры;
- δx. р – ширина зоны химической реакции.
Зная коэффициент температуропроводности среды:
время химической реакции:
имеем:
Выражение для фундаментальной скорости распространения пламени не учитывает влияние турбулентности среды, а также активных продуктов реакции на скорость химических превращений.
Представленная зависимость (Форм. 1) верна лишь для частного случая нормального распространения пламени, когда основной причиной его распространения является передача теплоты из зоны горения в свежую смесь.
При цепном механизме распространение пламени обусловлено только диффузией активных продуктов из зоны реакции в свежую смесь. Примером цепного распространения пламени может служить холодное пламя в смесях углеводородов с воздухом.
Распространение зоны горения путем умножения очагов самовоспламенения можно представить как воспламенение некоторых конечных объемов исходной или частично прореагировавшей горючей смеси нагретыми продуктами сгорания в процессе турбулентного перемешивания или как последовательное самовоспламенение конечных объемов горючей смеси, прошедшей определенную предпламенную подготовку.
Детонационное распространение пламени обусловлено сжатием горючей смеси в ударной волне. При этом необходимо, чтобы давление и температура во фронте ударной волны обеспечивали воспламенение горючей смеси с задержкой, не превышающей время пребывания смеси в зоне сжатия. Детонационное пламя представляет собой совместное распространение механической ударной волны с фронтом пламени. Скорость распространения детонационного пламени постоянна для определенных горючих смесей заданного состава и условий горения и составляет обычно 1 200-3 500 м/с.
Факторы, влияющие на воспламенение и горение
Температура и давление среды влияют не только на воспламеняемость и горючесть реагирующих смесей, они могут существенно изменить механизм процессов воспламенения и горения. Повышение температуры и давления в большинстве случаев увеличивает скорости реакций предпламенных превращений, что вызывает расширение пределов воспламенения, уменьшение температуры и периода задержки воспламенения, повышение скорости распространения пламени. Однако для сложных цепных реакций, как уже отмечалось выше, возможно несоблюдение этих закономерностей (см. рис. 1). В некоторых условиях развития сложных реакций повышение температуры и давления может ускорить обрыв цепей. При цепочно-тепловом воспламенении и низких давлениях существенную роль играют процессы зарождения, диффузии и гибели активных центров цепной реакции как в объеме, так и на стенках реакционного сосуда. Цепная реакция развивается медленно и основным фактором, определяющим саморазогрев, является цепное ускорение в процессе разветвления.
В области высоких давлений и температур очаги воспламенения возникают в результате быстрого и непрерывного перехода самоускорения цепного процесса в самоускорение, вызванное разогревом смеси. При высоких температурах становится возможным разрыв внутримолекулярных связей горючего и образование таким путем свободных радикалов, которые выполняют роль инициаторов развития цепной реакции. При относительно низкой температуре не может образоваться сразу значительного числа активных центров за счет разрыва межмолекулярных связей. Наблюдаются различные кинетические типы самовоспламенения. Например, для смесей углеводородов с воздухом возможны низкотемпературное многостадийное и низкотемпературное одностадийное самовоспламенение с замедленным развитием предпламенных реакций. Низкотемпературное многостадийное самовоспламенение протекает с последовательным образованием холодного, голубого и обычного горячего пламени.
Механизм химических предпламенных превращений смесей углеводородов с воздухом при относительно низких температурах можно представить следующей схемой.
В результате редких реакций окислительного распада углеводородов в объеме:
или гетерогенной реакции на стенках сосуда, вызывающей появление альдегидов R CHO:
образуется некоторое количество свободных радикалов.
Радикалы R—, реагируя с кислородом, дают перекисные радикалы:
Дальнейшие превращения перекисного радикала зависят от условий окисления. При температурах ниже ≈200 °C вероятно направление с образованием гидроперекисей и их превращениями:
Гидроперекиси распадаются с образованием свободных радикалов, дающих начало новым реакционным цепям. Например:
При температурах выше 200 °C более вероятным является изомеризация и распад перекисных радикалов по схеме:
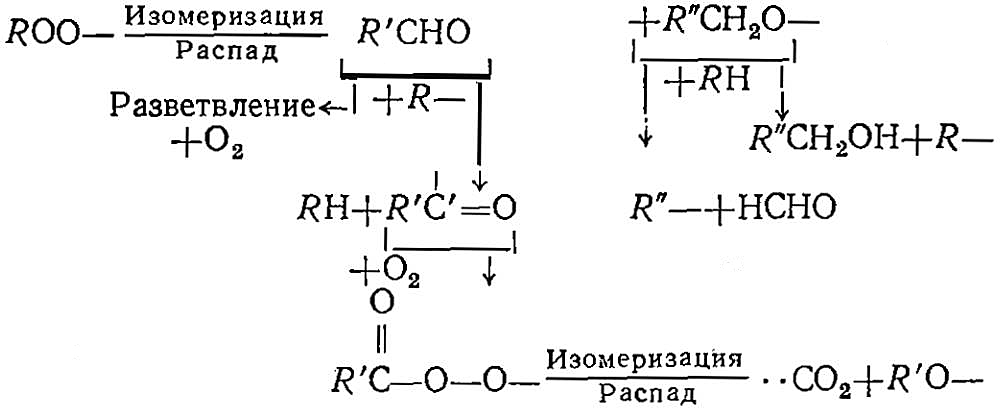
В этом направлении уже альдегиды играют роль основных активных промежуточных продуктов, вызывающих вырожденное разветвление.
При достаточно высоких начальных температурах и давлении зависимость скорости реакции от температуры:
наблюдается во всех встречающихся случаях цепочно-теплового воспламенения. Принимая во внимание эту наиболее общую черту кинетики процесса цепочно-теплового воспламенения, можно в процессе анализа и расчетов воспользоваться основными положениями теории теплового взрыва. Скорость реакции wx. р пропорциональна скорости повышения температуры реагирующей смеси wT:
где:
- – повышение температуры реагирующей смеси в ходе реакции;
- – изменение температуры в результате энергетического обмена реагирующей смеси с окружающей средой.
Зависимости T = T(τ) и TΣ = TΣ(τ) могут быть определены на основе расчета или экспериментально (рис. 3) путем непосредственного изменения температуры в процессе воспламенения T = T(τ) и измерения температуры горючей смеси при наличии всех форм энергетического обмена с окружающей средой, но в отсутствие химических реакций TΣ = TΣ(τ).

Поскольку:
то при постоянстве энергии активации на отдельных участках кривой T = T (τ) ее значение определяется выражением:
где:
- T – средняя температура на соответствующих участках кривой T = T (τ).
На основании экспериментальных данных установлена зависимость между основными параметрами цепочно-теплового воспламенения и условиями его осуществления:
где:
- τвс – период задержки воспламенения;
- A = f (α) – функция состава смеси;
- p – давление;
- Eэф – эффективная (средняя) энергия активации;
- Tвс – температура воспламенения.
Температура и давление горючей смеси существенно влияют на скорость распространения пламени. С увеличением температуры скорость распространения пламени увеличивается. Однако это увеличение не согласуется с ожидаемым значением скорости горения в соответствии с изменением скорости химических реакций:
Это обьясняется тем, что скорость распространения пламени определяется не только скоростью протекания реакций, а зависит также от температуропроводности среды. В турбулентной среде влияние температуры на скорость распространения пламени снижается в связи с тем, что повышение температуры уменьшает величину пульсационной скорости потока u′. Зависимость скорости распространения пламени от температуры в гетерогенных турбулентных смесях выражена более резко, чем в турбулентных гомогенных газовых смесях. Увеличение температуры гетерогенной смеси повышает скорости испарения и смешения.
В слабо турбулизированной среде чем выше давление, тем меньше нормальная скорость распространения пламени uн; это ухудшает характеристики горения. В сильно турбулизированной среде с повышением давления увеличивается пульсационная скорость потока u′, что, несмотря на уменьшение величины uн, увеличивает скорость горения.
Изучение влияния турбулентности среды имеет не только большое теоретическое значение для понимания сущности сложных физико-химических превращений в зоне пламени, но и очень важно для практики воздействия на процессы и регулирования их. Для осуществления рабочих процессов в Топливные системы высокого давления в судовых двигателяхдвигателях внутреннего сгорания широко используется создание организованного движения газа и турбулизация среды с целью регулирования скорости физико-химических процессов.
Процесс горения всегда осуществляется при той или иной степени турбулентности горючей смеси. Сам процесс горения сопровождается движением газа и оказывает воздействие на процессы воспламенения и горения.
Характеристики турбулентности влияют на процессы воспламенения и горения, изменяя и регулируя условия передачи теплоты и активных продуктов в процессах физико-химических превращений горючего и окислителя. Влияние их неоднозначно:
- в одних случаях они ускоряют эти процессы;
- в других затормаживают.
Так, с увеличением турбулизации горючей смеси расширяются пределы воспламенения, сокращается задержка воспламенения и повышается скорость распространения зоны горения, если при этом интенсифицируются процессы смешения паров горючего и окислителя, передачи теплоты и активных промежуточных продуктов в зоне реакции, не создаются условия гибели радикалов. Однако, если турбулизация способствует интенсивному отводу теплоты и активных продуктов из зоны реакции, ускоряет процесс гибели радикалов, т. е. вызывает охлаждение и снижение скоростей физических и химических превращений горючего и окислителя, эффект влияния будет противоположный. Особенно сильно влияет турбулентность среды на процессы распространения фронта пламени. Механизм действия турбулентности среды связан прежде всего с изменениями – искривлением и шероховатостью – поверхности фронта пламени. Характер искривления поверхности фронта пламени зависит от интенсивности и масштаба турбулентности.
На рис. 4 схематично показан фронт пламени при различных масштабе и степени интенсивности среды.
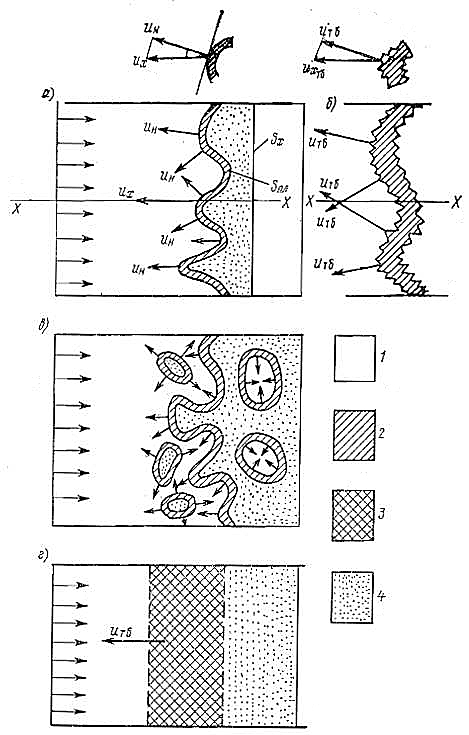
а – крупномасштабная турбулентность среды; б – мелкомасштабная турбулентность среды; в – большая интенсивность крупномасштабной турбулентности; г – объемная модель фронта пламени.
1 – свежая смесь; 2 – зона химических реакций; 3 – зона смешения и реакции; 4 – продукты сгорания
При крупномасштабной турбулентности l » δн (рис. 4, а) увеличивается поверхность фронта пламени. Наблюдаемая в заданном направлении x скорость распространения пламени ux увеличивается по сравнению с нормальной в таком отношении, как поверхность фронта пламени Sпл относится к площади ее проекции Sx, перпендикулярной направлению распространения:
Мелкомасштабная турбулентность l « δн вызывает появление шероховатости поверхности (рис. 4, б), при этом скорость распространения пламени uтб увеличивается благодаря интенсификации процессов переноса теплоты и вещества посредством микротурбулизации в самой зоне горения. В соответствии с выражением (Форм. 1) и учетом турбулентной диффузии aтб = u′ l имеем:
где:
- τтб – время горения в турбулентном слое фронта пламени.
При большой интенсивности турбулентности среды волнистость и шероховатость достигают такой величины, что от фронта пламени отрываются отдельные газовые объемы. Фронт пламени разрушается, появляются отдельные беспорядочно движущиеся объемы невоспламененной и горящей смеси (рис. 4, в). Объемы горящей смеси в продуктах сгорания и объемы продуктов сгорания в свежей смеси образуют при хаотическом движении широкую зону турбулентного пламени. Горение отдельных объемов свежей смеси происходит путем распространения пламени в них либо в результате самовоспламенения. Если применить для сложного фронта пламени при большой интенсивности различных турбулентных пульсаций понятие фундаментальной скорости в турбулентном потоке uтб, толщины зоны горения δтб и времени сгорания отдельных турбулентных газовых объемов τтб, то можно найти зависимости этих величин от u′, l и uн (рис. 4, г).
На основе экспериментальных данных установлено, например, что:
где:
- показатель m обычно больше n.
В условиях турбулентности, образованной прохождением потока через сетки:
- m ≈ 0,6 ÷ 1,0;
- n ≈ 0,2 ÷ 0,4.
При u′ » uн отдельные объемы турбулентной горючей смеси дробятся на части и время их горения:
а ширина зоны горения:
Очень сложная картина процессов воспламенения и горения наблюдается в турбулентной струе (факеле) распыленного в среде воздуха горючего.
В зоне горения факела с большим содержанием неиспарившегося горючего отчетливо наблюдаются следы горящих капель в виде ярко-желтых полос на сплошном голубом фоне факела пламени. При понижении температуры и уменьшении доли испарившегося горючего в смеси вид факела изменяется – голубой фон разрывается, непрерывный фронт пламени отсутствует, наблюдается горение отдельных капель и их совокупностей. При высоких температурах имеет место сплошной фронт пламени, а также очаги горения отдельных капель за этим фронтом.
Таким образом, для анализа процессов воспламенения и сгорания гетерогенной турбулентной горючей смеси очень важно оценить условия воспламенения горючей смеси, образованной вокруг капель, и скорость выгорания отдельных капель. Схема горения отдельной капли в потоке воздуха при кондуктивно-диффузионном механизме тепло- и массообмена и установившейся температуре капли показана на рис. 5.
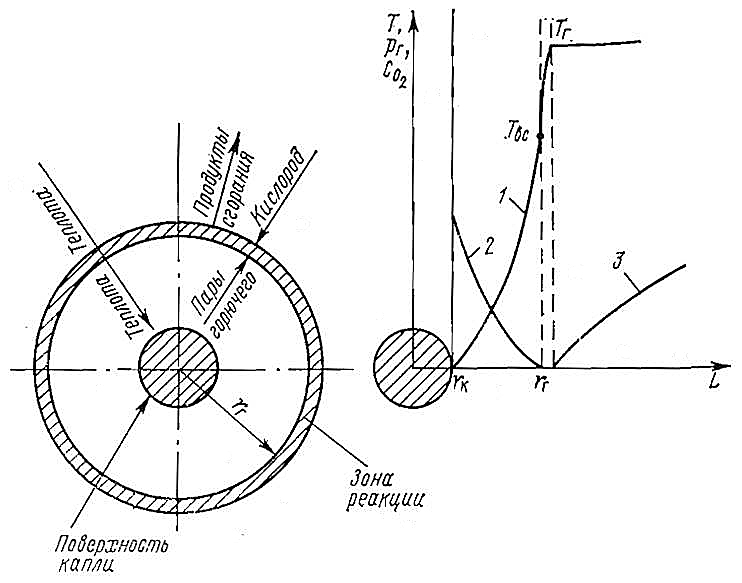
1 – температуры; 2 – давления паров топлива; 3 – концентрация кислорода
В таком идеальном случае вокруг капли устанавливается сферическая зона горения, к которой от капли диффундируют пары горючего, а из окружающей среды – кислород.
В процессе сгорания капель тяжелого топлива по мере фракционирования возможно явление ококсовывания поверхности капли. Тяжелые составляющие, подвергаясь нагреву, образуют на поверхности коксовый слой. В конце сгорания может остаться пористый остаток, состоящий из высокомолекулярных соединений либо из твердых коксовых остатков – продуктов термических превращении вещества капли. Количество несгоревшего топлива в виде коксового остатка сильно зависит от условий сгорания и свойств топлива.
Состав горючей смеси – соотношение компонентов горючего и окислителя оказывает влияние на развитие предпламенных превращений и последующие стадии процессов воспламенения и горения. Для начальных стадий предпламенных превращений в большинстве случаев благоприятные условия создаются в обогащенных смесях. Однако значительное обогащение с приближением к верхнему пределу воспламенения по причинам, указанным выше, ухудшает условия воспламенения и горения. Наиболее благоприятные условия для завершения воспламенения и развития процесса горения создаются при составах смеси α = 0,8 ÷ 0,9. В данном случае снижаются также затраты теплоты на диссоциацию, что способствует более эффективному использованию выделяющейся энергии в рабочих процессах двигателей.
Следует отметить положительное влияние на развитие процессов воспламенения неоднородности горючей смеси, в том числе и наличия жидкой фазы горючего. Присутствие различных местных концентраций создает благоприятные условия для отдельных стадий предпламенных превращений, так как некоторые из них нуждаются в богатых смесях, а другие в бедных смесях. В двухфазных смесях скорость распространения пламени слабо зависит от общего (суммарного) коэффициента избытка воздуха αΣ. Это объясняется тем, что процессы воспламенения и горения развиваются при переменных местных соотношениях коэффициентов состава смеси, в зонах вокруг отдельных капель.
Характеристики энергетических свойств, воспламеняемости и горючести
При оценке энергетических свойств горючего и горючих смесей необходимо определить тепловой эффект реакций горения, в результате которых происходит уменьшение внутренней химической энергии реагирующих веществ с выделением теплоты и изменением их объема. Величина теплового эффекта зависит от свойств горючей смеси и условий протекания реакций – температуры, давления и объема.
Если реакция протекает при постоянном давлении, то уменьшение внутренней химической энергии сказывается не только на величине теплового эффекта Qp, но и на внешней работе L. В случае развития процесса при постоянном объеме внешняя работа равна нулю, а уменьшение внутренней энергии определяет только величину теплового эффекта реакции QV + L. Тепловые эффекты Qp и QV связаны соотношением QV = Qp. Тепловой эффект химического процесса при V = const больше, чем при p = const, на величину работы, затрачиваемую на расширение газа.
Теплота сгорания – количество теплоты, выделяющейся при полном сгорании единицы массы или объема горючего в кислороде воздуха, является важнейшим показателем его энергетических свойств. Тепловой эффект реакции между горючим и окислителем (завершается образованием наиболее устойчивых окислов), отнесенный к единице массы или объема всего реагирующего количества смеси, называют теплотой сгорания горючей смеси. Теплота сгорания (теплопроизводительность) горючей смеси оценивает энергетические свойства данной пары горючего и окислителя. При определении теплоты сгорания необходимо учитывать условия, к которым относится тепловой эффект.
Продукты сгорания могут находиться в различном агрегатном состоянии, и теплота их образования будет неодинакова. Различают высшую и низшую теплоту сгорания (теплопроизводительность). Высшая теплота сгорания включает, а соответственно низшая не включает количество теплоты, которое выделяют продукты сгорания, конденсирующиеся в условиях определения.
Теплота сгорания горючей смеси и горючего определяются на основе анализа уравнения горения. При сжигании углеводородного горючего в воздухе оно имеет вид:
где:
- CnHmOpSe и NuOV – условные химические формулы горючего и воздуха;
- μ0 – теоретическое количество воздуха, необходимого для полного сгорания горючего, моли на 1 моль.
Из уравнения (Форм. 2) следует:
В соответствии с законом Гесса тепловой эффект реакции (Форм. 2) определяется суммой теплот образования исходных и конечных продуктов:
Величина QM представляет теплоту сгорания исходной смеси горючего и воздуха, взятых в стехиометрическом соотношении (1 моль горючего и μ0 молей воздуха). Следовательно, теплота сгорания 1 кг смеси горючего и воздуха равна:
а теплота сгорания горючего:
где:
- Mг и Mв – молекулярные массы горючего и воздуха.
Для расчета теплоты сгорания горючего можно воспользоваться также следующими выражениями.
Теплота сгорания горючего, отнесенная к единице массы:
где:
- AC, AH, AS – атомные массы углерода, водорода и серы.
Учитывая, что теплота образования при 298,15 °K CO2, H2O (газ) и SO2 соответственно составляет 393,5; 241,8 и 296,4 кДж/(г·моль), находим низшую теплоту сгорания горючего:
По известной формуле Д. И. Менделеева низшая теплота сгорания углеводородного горючего:
Теплопроизводительность смеси углеводородного горючего и воздуха:
где:
- – теоретически необходимое количество воздуха, кг на 1 кг горючего;
- Cг, Hг, Sг, Oг – содержание в горючем углерода, водорода, серы и кислорода, %.
На эффективность использования запаса энергии Oсм влияют термодинамические свойства продуктов сгорания. Эти свойства зависят от их теплоемкости, молекулярной массы, и могут характеризоваться величиной газовой постоянной. В практике удобно оценивать эти свойства по таким показателям, как температура горения, степень диссоциации и степень газообразования.
Теоретическая температура горения:
где:
- cΣ – теплоемкость продуктов сгорания.
Степень газообразования – объем газов при нормальных условиях, образующихся при сжигании единицы массы горючего, v0, м3, в соответствии с уравнением (Форм. 2):
где:
- 22,4 – объем, занимаемый 1 кг·молем вещества при нормальных условиях, м3.
Воспламеняемость характеризуют свойства, от которых зависят пределы воспламенения, температура и период задержки воспламенения, склонность к низкотемпературным превращениям, энергия активации.
Пределы воспламенения углеводородов (C > 3) в воздухе мало изменяются в зависимости от строения и молекулярной массы (табл. 1).
| Таблица 1. Пределы воспламенения в воздухе некоторых горючих веществ при температуре 20 °C | |||||
|---|---|---|---|---|---|
| Вещество | Пределы воспламенения, % по объему | Вещество | Пределы воспламенения, % по объему | ||
| нижний | верхний | нижний | верхний | ||
| Водород | 4,0 | 74,2 | Бутан | 1,9 | 8,4 |
| Ацителен | 2,5 | 80,0 | Гексан | 1,3 | 6,9 |
| Окись этилена | 3,0 | 80,0 | Гептан | 1,0 | 6,0 |
| Этиловый эфир | 1,9 | 36,5 | Циклогексан | 1,3 | 8,4 |
| Окись углерода | 12,5 | 74,2 | Бензол | 1,4 | 6,8 |
| Этилен | 2,8 | 28,6 | Толуол | 1,3 | 6,8 |
| Бутилен | 1,7 | 9,0 | Авиабензины Реактивное топливо | 0,80-1,0 1,0-1,4 | 5,5-7,0 6,0-7,1 |
В области низких давлений и для богатых смесей они имеют несколько выраженных минимумов на кривой αпр = f (p) (рис. 6).
1 – метан; 2 – бутан; 3 – н-гексан
Это обусловлено рассмотренными выше особенностями развития в таких условиях цепного процесса. Широкие пределы воспламенения имеют водород и ацетилен. Пределы воспламенения оценивают и такие показатели, как низший и высший температурные пределы, представляющие собой температуру жидкого горючего, при которой концентрация паров над поверхностью соответствует пределам воспламенения. Низший температурный предел воспламенения соответствует понятию «температура вспышки». Эти показатели больше характеризуют пожарную опасность горючего.
Температура и период задержки воспламенения сильно зависят от строения и молекулярной массы горючего. Указанные зависимости для некоторых углеводородов и их смесей можно проследить на рис. 7 и 8.
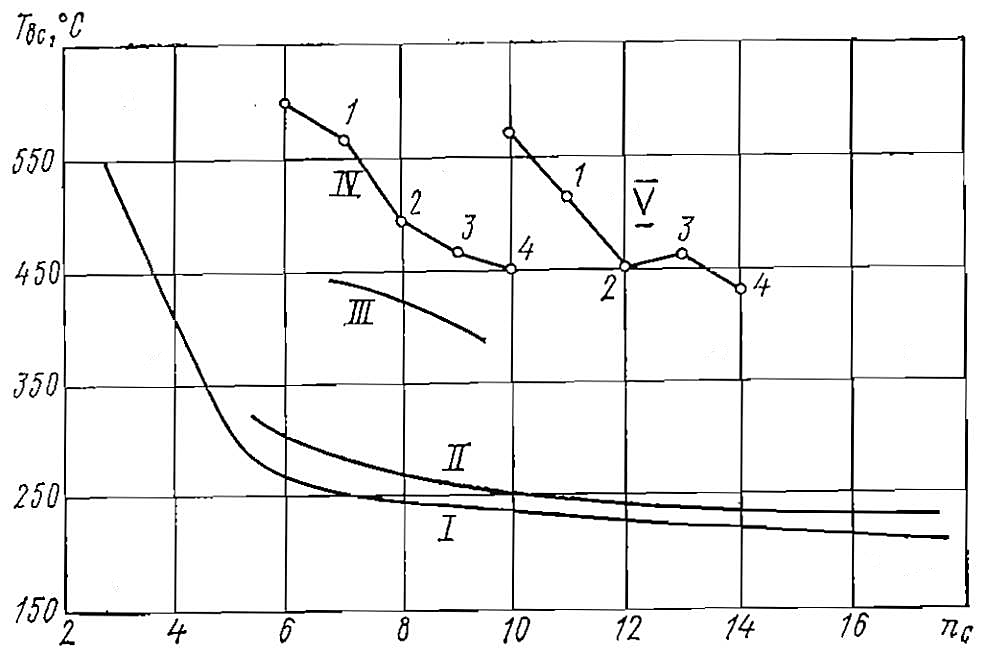
I – алканы; II – алкены; III – изо-алканы; IV и V – моно- и бициклические ароматические углеводороды соответственно.
1-4 – число атомов углерода в алкильных цепях
Энергия активации зависит не только от вида горючего и окислителя, но и от условий воспламенения. Изменение энергии активации с переходом из одной температурной области в другую связано с механизмом разветвления цепной реакции и дает важную информацию о предпламенных реакциях. Сложность и одновременность протекания различных предпламенных превращений позволяют определить лишь некоторую среднюю эффективную энергию активации.
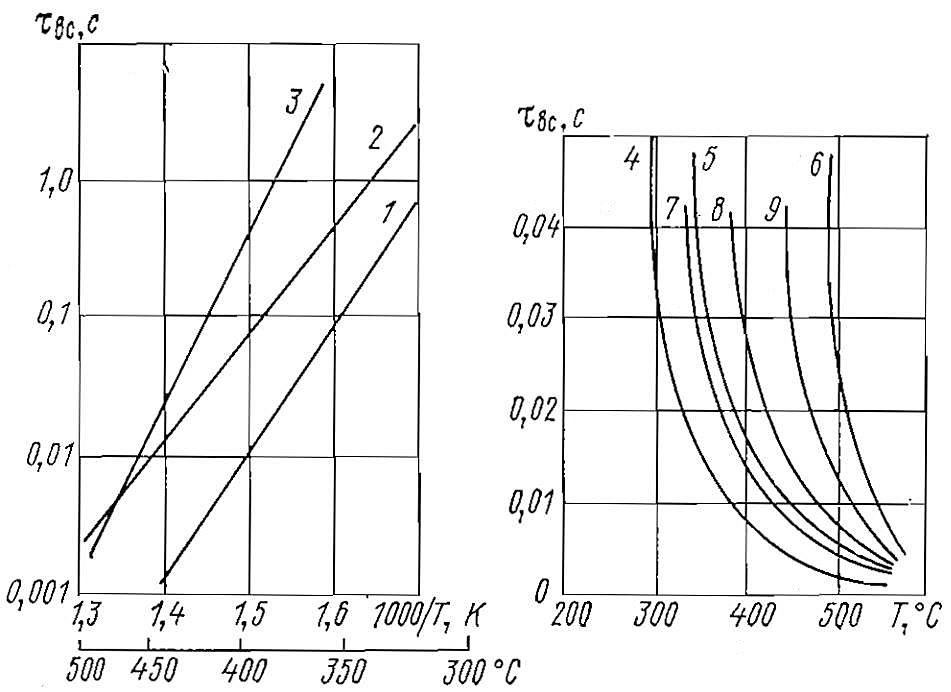
1 – гептан (Е = 167 кДж/(г·моль)); 2 – изо-октан (Е = 134 кДж/г·моль); 3 – бензол (Е = 256 кДж/(г·моль)); 4 – цетан; 5 – 35 % цетана и 65 % α-метилнафталина; 6 — α-метилнафталин; 7, 8, 9 – соответственно алканоциклановая, циклановая и ароматическая фракции дизельного топлива
Характеристики горючести включают физико-химические свойства, от которых зависят скорость распространения фронта пламени и температура в его зоне. Они могут быть выражены фундаментальной (нормальной) скоростью распространения пламени и температурой горения. Чем выше реакционная способность горючего с данным окислителем, больше энергетический запас реагирующей смеси (тепловой эффект реакции) и меньше молекулярная масса продуктов сгорания, тем выше скорость и температура горения.
Некоторые общие зависимости между строением, молекулярной массой и фундаментальной скоростью распространения пламени углеводородов в воздушной среде показаны на рис. 9.
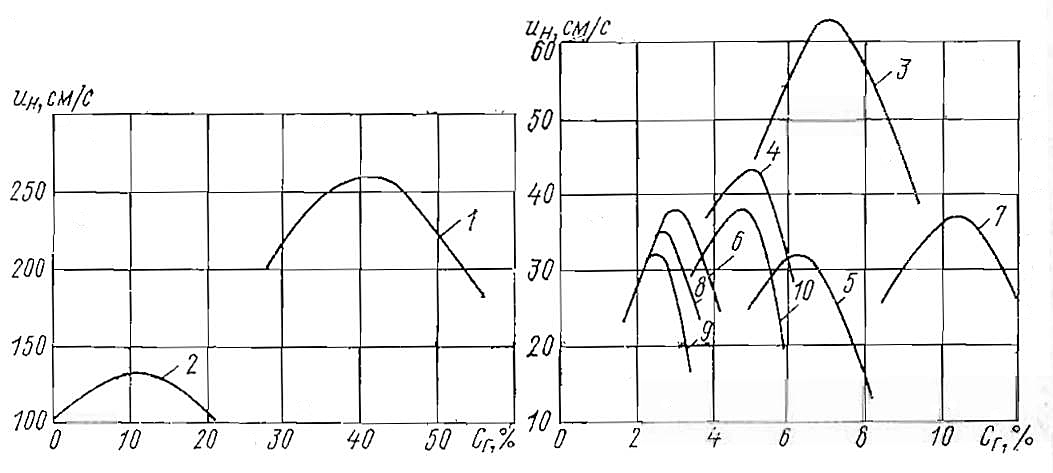
1 – водород; 2 – ацетилен; 3 – этилен; 4 – пропилен; 5 – ацетон; 6 – бензол; 7 – метан; 8 – циклогексан; 9 – гексан; 10 – этиловый эфир
Скорость распространения пламени может возрастать при добавлении небольших количеств некоторых соединений, а также при смешении нескольких компонентов. Напротив, некоторые вещества и инертные газы снижают скорость распространения пламени. Нормальная скорость распространения пламени увеличивается с повышением температуры и понижением давления. Эти зависимости имеют следующий вид:
- ;
- ;
В интервале температур T = 200 ÷ 890 К в среде воздуха для углеводородов можно принять:
- n ≈ 2;
- a = 10;
- b = 3,4 · 10-4;
- m = 0,1 ÷ 0,5.
Температура горения углеводородов в воздухе составляет Tгор = 2 000 ÷ 3 000 К.
Рассмотренные общие характеристики воспламеняемости и горючести еще недостаточно оценивают способность горючего обеспечивать эффективный рабочий процесс в различных типах двигателей. Поэтому необходимо изучить некоторые специфические эксплуатационные свойства для отдельных групп горючего.
Особенности воспламенения и сгорания в двигателях
Для рабочего процесса поршневых двигателей с принудительным воспламенением необходимо следующее:
- приготовление однородной бензино-воздушной смеси до начала воспламенения и горения;
- принудительное поджигание рабочей смеси в конце ее сжатия.
Горючая смесь, поступающая через впускную систему, смешивается в цилиндре двигателя с оставшимися продуктами сгорания, при этом образуется рабочая смесь. В процессах ее превращения можно выделить три фазы:
- зажигание и формирование очага пламени;
- распространение турбулентного пламени по всей камере сгорания;
- догорание отдельных объемов рабочей смеси, образующихся при разрушении фронта пламени в конце горения.
Продолжительность развития первой фазы зависит от мощности источника зажигания, состава смеси и фундаментальной скорости распространения пламени. Первая фаза завершается появлением очага пламени такого размера, при котором возможно воздействие на него крупномасштабной турбулентности.
Во второй фазе решающее значение приобретает ускорение горения за счет турбулентности, при этом меньше сказывается влияние состава смеси и физико-химических свойств горючего. Под воздействием турбулентных пульсаций фронт пламени становится волнистым и шероховатым, а в конце сгорания распадается на отдельные очаги горения. Время догорания таких очагов зависит от состава смеси и фундаментальной скорости распространения пламени.
Средняя скорость распространения зоны горения составляет в зависимости от конструкции камеры сгорания и режима работы двигателя 15-40 м/с. В некоторых условиях нормальное сгорание нарушается. Известны два вида нарушений: неуправляемое горение в результате воспламенения рабочей смеси от нагретых поверхностей или частиц нагара и детонационное горение.
Сильно нагретые части в камере сгорания — электроды свечи, выпускной клапан, а также тлеющий нагар и взвешенные частицы нагара могут служить источниками воспламенения и вызвать неуправляемое воспламенение и горение рабочей смеси.
Детонационное горение представляет особый вид горения, отличающийся механизмом и скоростью распространения пламени. При детонационном горении развитие первой и начало второй фаз осуществляется так же, как при нормальном процессе. После прохождения фронтом пламени значительной части камеры сгорания наблюдается некоторое замедление его продвижения, после чего остальная часть рабочей смеси сгорает чрезвычайно быстро за время порядка 3 · 10-4 с. Горение в этой части происходит неравномерно и сопровождается местными повышениями температуры и давления. Схема протекания детонационного горения (рис. 10) такова.
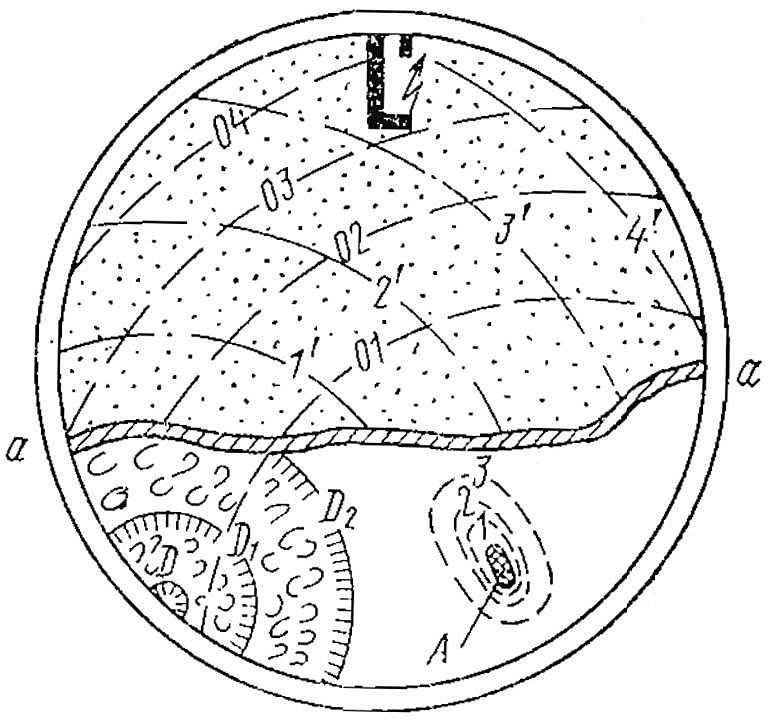
а — а — положение фронта пламени к началу детонации; А – очаг самовоспламенения.
1-3 – мгновенные положения распространения зоны горения от очага А; 01, 02, 03, 04 — ударные волны; 1′, 2′, 3′, 4′ – отраженные ударные волны;
D, D1, D2 – возникновение и распространение детонационных волн
В рабочей смеси еще до воспламенения в течение ходов наполнения и сжатия развиваются предпламенные химические реакции. Наиболее благоприятные условия развития реакций создаются уже в процессе горения в рабочей смеси, которая должна сгорать в последнюю очередь. В определенной части этой смеси развитие предпламенных химических превращений может завершиться самовоспламенением в одном или нескольких очагах вследствие неоднородности реагирующей смеси по составу и температуре. От очагов самовоспламенения по предварительно подготовленной химически активной смеси распространяется зона горения со скоростью, достигающей звуковой и выше. За счет передачи теплоты и активных продуктов такие скорости горения получить нельзя. В этом случае имеет место последовательное самовоспламенение смежных объемов активной смеси.
Распространение зоны горения со скоростью, превышающей скорость звука, приводит к образованию ударных волн. Обычно ударные волны не вызывают появления детонационного распространения пламени. Однако вследствие отражения ударных волн от стенок и их наложения при условии, что в местах их прохождения имеется еще не прореагировавшая полностью смесь, возможно возникновение детонационной волны. По свежей смеси такая волна может распространяться со скоростью 2 000-2 400 м/с, а по частично прореагировавшей смеси – со скоростью 1 500-1 800 м/с. Ударные волны в продуктах сгорания распространяются со скоростью 1 200-1 300 м/с.
Стук в двигателе, работающем с детонацией, представляет собой колебания стенок цилиндров, которые вызываются прямыми и отраженными ударными волнами. Колебание газов сохраняется в течение значительной части хода расширения. Массовый поток газов усиливает теплоотдачу от газа к стенкам. Большой отвод теплоты через стенки цилиндра вызывает их перегрев, понижение температуры выпускных газов и увеличение расхода горючего. Для количественной оценки интенсивности детонационного горения можно использовать любой признак его проявления. Чаще всего характер детонации в двигателе оценивается по температуре головки или стенок цилиндра, интенсивности и частоте колебаний газов и звуковому эффекту.
Влияние конструктивных и эксплуатационных факторов на рабочий процесс двигателя связано прежде всего с изменением температуры, давления, состава реагирующей смеси, гидродинамических характеристик среды и времени, предоставляемого для развития отдельных стадий воспламенения и горения.
Если при изменении какого-либо фактора в рабочей смеси в период, предшествующий ее горению, повышаются температура и давление, увеличивается время предпламенных превращений, не уводятся из зоны реакции активные продукты, то вероятность возникновения детонационного сгорания увеличивается.
Возможность возникновения детонации и ее интенсивность зависят от свойств горючей смеси. Для бензинов различного химического состава под влиянием того или иного фактора интенсивность детонационного горения изменяется не в одинаковой степени. Это обусловлено характером развития предпламенных реакций и видом активных промежуточных продуктов, вызывающих разветвление цепных реакций. Например, с изменением температуры более резко меняется интенсивность детонации ненасыщенных и ароматических углеводородов, чем для алканов и цикланов. Ароматические углеводороды имеют высокие детонационные характеристики на богатых смесях и в условиях наддува, а изо-алканы – на несколько обедненных смесях без наддува.
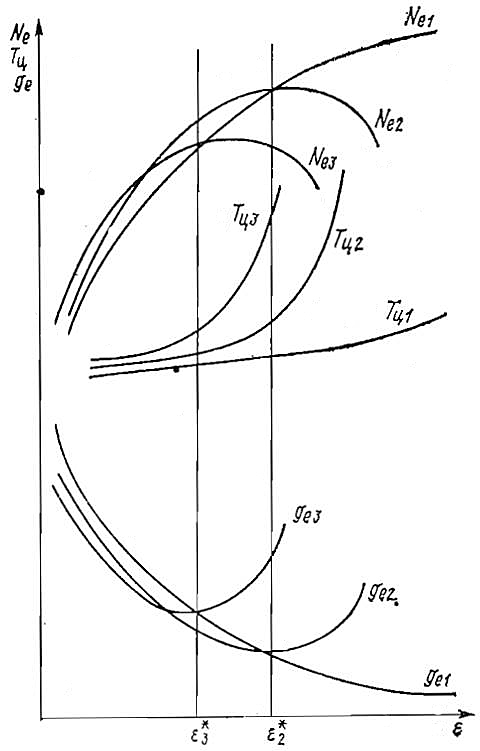
С изменением любого фактора, вызывающего детонацию в двигателе, пока интенсивность ее мала, мощность и экономичность двигателя снижаются незначительно, а на преддетонационных режимах даже увеличиваются. Только при сильной детонации мощность двигателя резко снижается, а расход топлива увеличивается (рис. 11).
Рассмотрим влияние на процессы горения некоторых факторов.
С повышением степени сжатия, по крайней мере до 15, увеличиваются эффективный КПД и мощность двигателя. Чем больше степень сжатия, тем выше температура и давление рабочей смеси. При недостаточной детонационной стойкости горючего это вызовет детонационное горение, интенсивность которого будет возрастать по мере повышения степени сжатия (см. рис. 11).
С увеличением угла опережения зажигания жесткость работы и мощность двигателя повышаются, если горючее обеспечивает нормальное сгорание. Выше оптимального значения угла опережения зажигания мощностные и экономические показатели работы двигателя ухудшаются. Чем больше угол опережения зажигания, тем выше давление и температура смеси, сгорающей в последнюю очередь, поэтому легче возникает детонация и выше интенсивность этого процесса.
Если Процесс сгорания топлива в цилиндре дизеляпроцесс горения развивается нормально, то максимальная мощность двигателя достигается при α = 0,84 ÷ 0,9. При таких составах смеси наибольшее количество теплоты выделяется при сжигании смеси с учетом диссоциации продуктов сгорания и наблюдается наибольшая скорость распространения пламени. Сильное обогащение смеси при α < 0,8 снижает мощность двигателя в результате значительного понижения теплоты сгорания рабочей смеси, температуры и скорости горения. Минимальный удельный расход при нормальном горении и максимальное использование теплоты сгорания горючего имеет место при α = 1,05 ÷ 1,10.
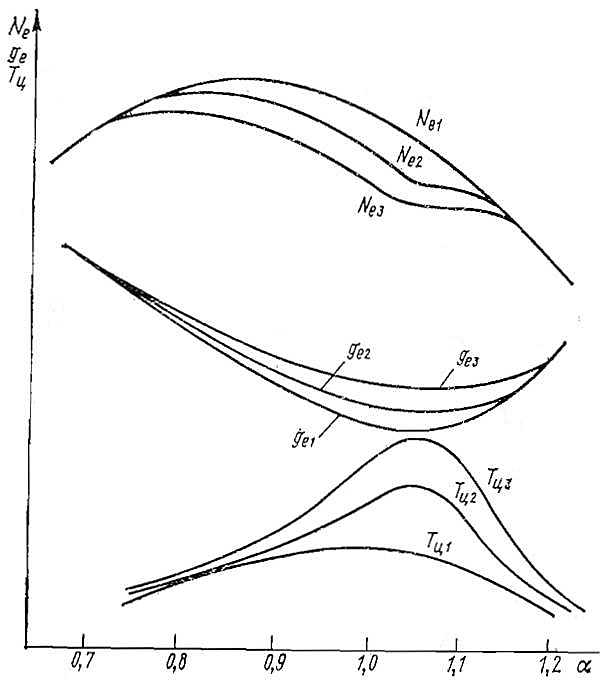
С обеднением смеси понижается температура расширяющихся газов за счет избыточного воздуха, увеличивается содержание двухатомных газов O2, N2 в продуктах сгорания, что улучшает их термодинамические свойства. По мере обеднения смеси скорость горения уменьшается, это приводит к уменьшению коэффициента использования теплоты сгорания. Максимальная средняя температура газов в цилиндре и связанная с этим наиболее высокая тепловая напряженность камеры сгорания и поршня, а следовательно, и наибольшая склонность к детонации достигаются при α = 1,0 ÷ 1,05. С обогащением и обеднением рабочей смеси относительно этого состава склонность к детонации и ее интенсивность снижаются (рис. 12).
С увеличением частоты вращения коленчатого вала двигателя усиливается турбулентность среды, повышается содержание в рабочей смеси остаточных газов, уменьшается время протекания горения и возрастает его скорость, но повышаются температура и давление. В целом увеличение частоты вращения коленчатого вала уменьшает возможность детонационного горения.
Двигатель с воспламенением от сжатия. Рабочий процесс дизеля имеет следующие особенности:
- смесеобразование осуществляется непосредственно в камере сгорания в весьма короткие промежутки времени, процессы подачи и смещения не завершаются к началу воспламенения, а продолжают развиваться одновременно с основными стадиями горения;
- горючее воспламеняется без внешнего источника зажигания в среде воздуха, сильно нагретого за счет сжатия в цилиндре двигателя, воспламенение и горение происходит в гетерогенной смеси, когда часть горючего находится в паровой фазе, а часть в жидкой фазе.
С началом воспламенения процессы смесеобразования не успевают завершиться во всем объеме камеры и протекают одновременно с процессом горения основной части впрыснутого горючего. При этом вследствие повышения температуры и давления скорости физико-химической подготовки еще не участвующего в горении топлива увеличиваются. В дальнейшем условия горения ухудшаются. В результате фракционирования при испарении капель в последнюю очередь испаряются и участвуют в горении углеводороды большой молекулярной массы и тяжелые гетероорганические соединения. Замедление горения в стадии догорания обусловлено также недостаточным поступлением кислорода воздуха в зону реакции. При высокой температуре и недостаточном подводе кислорода химические превращения гетерогенной горючей смеси протекают с образованием продуктов неполного сгорания, в том числе и частиц сажи. Дымление на выпуске является характерной чертой работы дизеля на режимах больших нагрузок.
В едином непрерывном комплексе физико-химических превращений топлива в дизеле можно выделить стадии, имеющие некоторые особенности в развитии.
К первой стадии относятся процессы, протекающие от начала впрыска до образования начальных очагов воспламенения, что соответствует нарастанию давления на индикаторной диаграмме. Эта стадия называется периодом задержки воспламенения. Физико-химические превращения топлива в этой стадии:
- распыливание,
- испарение,
- смешение,
- предпламенные химические реакции развиваются в условиях относительно низких температур и давления.
В сильно обогащенных зонах и частично в жидкой фазе протекают реакции в направлении обычного окисления с образованием гидроперекисей, альдегидов, сложных эфиров и других кислородных соединений. В определенных температурных интервалах предпламенные превращения развиваются по типу холоднопламенного процесса. Глубокие предпламенные химические превращения проходят в относительно небольшой части топливно-воздушной смеси на периферии факела и завершаются цепочно-тепловым воспламенением.
При хорошей воспламеняемости горючего, высокой температуре и давлении в камере сгорания предпламенные процессы в гетерогенной горючей смеси развиваются достаточно быстро и успевают завершиться с образованием начальных очагов воспламенения еще на ранних стадиях развития факела впрыскиваемого топлива. Наиболее благоприятные условия воспламенения создаются на периферии факела, где и появляются начальные очаги горения. В неблагоприятных условиях в результате медленного развития предпламенных реакций значительная часть топлива успевает испариться и смешаться с воздухом, а это, в свою очередь, ухудшает условия воспламенения; цепочно-тепловой взрыв осуществляется одновременно в нескольких очагах.
Сущность второй стадии заключается в распространении турбулентного горения по топливо-воздушной смеси, образованной при испарении мелких капель на периферии факела и в районах скопления капель. Скорость распространения зоны пламени зависит от степени подготовки смеси в ходе одновременно протекающих процессов распиливания, испарения, смешения и предпламенной химической подготовки.
После образования первоначальных очагов воспламенения и начавшегося турбулентного горения возможно возникновение новых очагов воспламенения, от которых в свою очередь распространяется турбулентный фронт пламени.
Если предпламенная физико-химическая подготовка развивается с большой задержкой и в большом объеме гетерогенной смеси, то практически одновременно возникает большое количество начальных очагов воспламенения. В таких условиях зона реакции может распространяться в результате их самоумножения – последовательного самовоспламенения предварительно подготовленной горючей смеси. Такой вид горения обычно вызывает высокую скорость нарастания давления и двигатель работает жестко.
В третьей стадии догорания горение в известной степени регулируется характеристиками подачи и турбулентности среды. Несмотря на высокие температуру и давление, воспламенение и горение развиваются в диффузионной области. Увеличение концентрации продуктов сгорания и уменьшение концентрации кислорода тормозит протекание химических процессов, решающее значение приобретает турбулентный тепло и массообмен в зонах горения.
Факторы, влияющие на воспламенение и горение. Основными параметрами воспламенения и горения в дизеле являются:
- период задержки воспламенения,
- скорость нарастания давления,
- максимальное давление сгорания и продолжительность горения.
Изменение свойств топлива и условий воспламенения и горения вызывает соответствующие изменения этих параметров, а следовательно, мощности и удельного расхода топлива.
Увеличение степени сжатия в дизеле, как и в карбюраторном двигателе, вызывает повышение мощности и улучшение экономичности. Однако возможность возникновения нарушений в рабочем процессе, напротив, уменьшается. Чем выше степень сжатия, тем меньше период задержки воспламенения и ниже скорость нарастания давления, а следовательно, более плавно работает двигатель. При небольшой степени сжатия наблюдается жесткая работа. Анализ зависимостей периода задержки воспламенения и скорости нарастания давления от степени сжатия (рис. 13) показывает, что влияние химического состава топлива на параметры рабочего процесса сказывается тем сильнее, чем меньше степень сжатия.
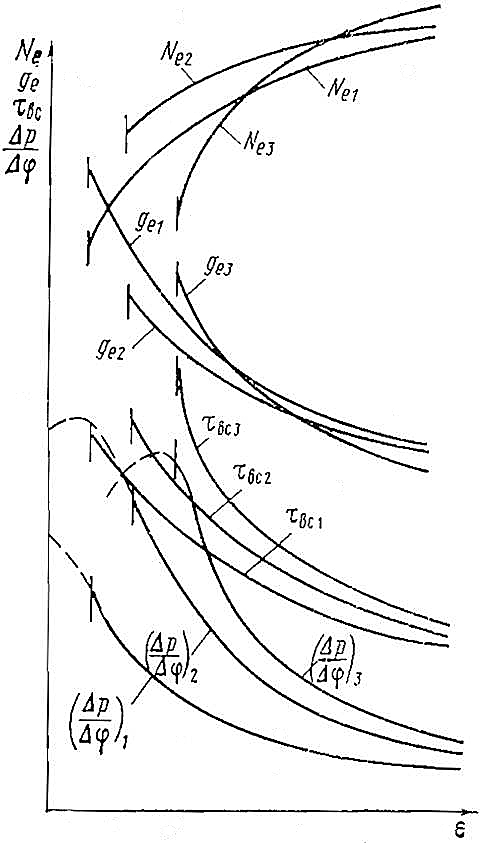
Кривые с индексами 1, 2, 3 – топлива различной воспламеняемости xвс: xвс1 > xвс2 > xвс3
Наддув в дизеле повышает его мощность, сокращает период задержки воспламенения. Положительное влияние наддува на рабочий процесс двигателя будет сказываться при условии сохранения оптимальных параметров распыливания, распределения топлива в камере сгорания и турбулентности среды.
Коэффициент избытка воздуха, определяемый нагрузкой дизеля, мало влияет на скорость развития процессов воспламенения и горения в дизеле, поскольку они осуществляются при местных непрерывно меняющихся составах рабочей смеси. С увеличением нагрузки двигателя общий коэффициент избытка воздуха снижается. При этом увеличивается тепловая напряженность, повышается температура газов и стенок камеры сгорания, что уменьшает период задержки воспламенения.
Угол опережения впрыска топлива влияет на длительность задержки воспламенения и скорость нарастания давления. Чем позднее впрыскивается топливо, тем выше и температура воздуха в момент подачи, а следовательно, меньше период задержки воспламенения и скорость нарастания давления. При слишком позднем впрыске предпламенные процессы частично переносятся на такт расширения, когда температура и давление начинают снижаться, а это увеличивает период задержки воспламенения. Максимальное давление сгорания при этом резко падает вследствие увеличения объема камеры сгорания. Процесс горения разбивается плавно, но с малой эффективностью.
С увеличением частоты вращения коленчатого вала усиливается вихревое движение, повышаются температура и давление воздуха в камере сгорания, а также давление распыливания. Все это благоприятно сказывается на ходе подготовки топлива к воспламенению, хотя время протекания процессов сокращается.
Форма, размеры и материал камеры сгорания оказывают значительно большее влияние на рабочий процесс дизеля, чем это наблюдается в карбюраторном двигателе. Это объясняется тем, что, изменяя условия воспламенения и сгорания за счет этих факторов, можно добиться значительно большего регулирования физических и химических превращений гетерогенной смеси, чем это возможно для гомогенной горючей смеси. Этим объясняется также чрезвычайно большое разнообразие конструкций камер сгорания. За счет специальных систем смесеобразования, особенно в разделенных камерах сгорания, оказывается возможно значительно уменьшить влияние свойств топлива на воспламенение и горение и создать на основе дизеля многотопливные двигатели.
Примером таких систем смесеобразования являются дизели с пленочным смесеобразованием. Для сокращения количества топлива, участвующего в начальном воспламенении, а следовательно, сокращения периода задержки воспламенения и скорости нарастания давления и дымности выпускных газов, в объем камеры сгорания впрыскивается обычным способом около 5 % топлива от цикловой подачи. Остальная часть топливного заряда подается на нагретые стенки камеры сгорания, где осуществляется предварительная предпламенная химическая подготовка. Интенсивным вихревым движением воздуха топливо распределяется тонкой пленкой на стенках и по мере испарения смешивается с кислородом воздуха. При этом образуется достаточно подготовленная горючая смесь, содержащая активные продукты в результате термоокислительной подготовки на нагретой поверхности камеры. В таких условиях эффективно сгорают топлива различного фракционного и группового углеводородного состава, в том числе и бензины.
Нормальной считается работа дизеля, когда высокие мощностные и экономические показатели достигаются при достаточно плавном нарастании давления, величина которого в зависимости от конструкции и предназначения дизеля составляет от 0,2 до 1,0 МПа на один градус поворота коленчатого вала (п. к. в.). При большей скорости нарастания давления силовые нагрузки на основные детали шатунно-кривошипных групп резко возрастают, двигатель работает жестко со стуком. Это снижает срок службы двигателя.
Повышение до определенных пределов жесткости работы повышает мощность и экономичность, так как термодинамические условия процесса улучшаются, горение основной части топливного заряда протекает при V ≈ const. Очень жесткая работа вызывает снижение мощности и увеличение удельного расхода топлива. Чем меньше длительность задержки воспламенения, тем меньше жесткость работы и тем легче регулировать процесс горения путем изменения характеристик впрыска и других факторов, влияющих на процессы испарения и смешения в цилиндре двигателя.
Быстрое завершение стадии начального воспламенения, хотя и благоприятно с точки зрения улучшения пуска, ухудшает условия развития последующих стадий горения. В результате небольшой задержки воспламенения включающаяся в горение рабочая смесь не имеет достаточной физико-химической подготовки, поэтому скорость горения снижается. Процесс горения протекает плавно, но замедленно, при увеличивающемся объеме.
Газотурбинные двигатели. К особенностям горения в этих двигателях можно отнести:
- непрерывность процесса горения при постоянном давлении в быстро движущемся потоке воздуха;
- высокую тепловую напряженность процесса, вызванную сжиганием в ограниченном объеме большого количества топлива. Для обеспечения устойчивого горения в камерах сгорания устанавливаются стабилизаторы:
- завихрители;
- экраны;
- обтекатели.
В камерах сгорания можно выделить три зоны. В первой осуществляется распыливание топлива, смешение с воздухом и образование горючей смеси с коэффициентом избытка воздуха около единицы. В эту зону поступает только часть воздуха, подаваемого в камеру сгорания. Во второй зоне происходит воспламенение и горение и подается некоторое количество воздуха. Образовавшиеся газы имеют высокую температуру и не могут направляться непосредственно на лопатки турбины. Поэтому в третьей зоне продукты сгорания смешиваются с воздухом, получают упорядоченное движение и поступают далее в направляющий аппарат, а затем на лопатки газовой турбины с температурой 800-900 °C, обеспечивающей ее высокую надежность.
Основным нарушением процесса горения в газотурбинном двигателе является срыв пламени и вибрационное горение.
Причинами срыва пламени и вибрационного горения могут быть нарушения в работе топливоподающей аппаратуры, резкие изменения давления и температуры воздуха на входе в камеру сгорания. Особенно неблагоприятные условия для протекания процесса горения создаются при понижении температуры и давления воздуха.
При некоторых нарушениях в подаче топлива или процесса горения возникают колебания давления в камерах сгорания, которые, усиливаясь, могут привести к срыву пламени.
Присадки для улучшения воспламеняемости и горючести
Присадки-антидетонаторы. Антидетонаторами называют вещества, добавление которых в небольшом количестве повышает детонационную стойкость бензина. Наиболее эффективными являются металлоорганические соединения свинца, марганца и железа (табл. 2).
| Таблица 2. Физические свойства металлоорганических антидетонаторов | ||||
|---|---|---|---|---|
| Антидетонатор | Плотность при 20 °C, г/см | Температура, °C | Давление насыщенных паров, при 38 °C, мм рт. ст. | |
| кипения | плавления | |||
| Тетраэтилсвинец (C2H5)4Pb | 1,652 | 200 | -130 | 0,3 |
| Тетраметилсвинец (CH3)4Pb | 1,995 | 110 | -28 | 26,5 |
| Циклопентадиенил-трикарбонил марганца C3H5Mn(CO)3 (ЦТМ) | – | – | +76-77 | – |
| Метилциклопентадиенилтрикарбонаты марганца C6H7Mn(CO)3 (МЦТМ) | 1,39 | 233 | -1,5 | – |
| Пентакарбонилжелезо Fe(CO)5 (ПКЖ) | 1,457 | 102,5 | -21 | – |
Действие антидетонаторов на основе металлов проявляется только при температурах выше порога их термической стабильности. Распад антидетонатора сопровождается выделением высокоактивного атомарного металла.
При термическом распаде антидетонаторов типа Me (R)n по схеме:
образуются свободные радикалы. Они должны ускорять реакцию окисления, но этого не наблюдается. Удовлетворительного объяснения этого явления с точки зрения цепной теории не существует. Возможно, что радикалы реагируют друг с другом с образованием углеводородов.
Для эффективных антидетонаторов характерно наличие прямых связей между атомами углерода и металла. Именно эта связь обеспечивает образование активного атомарного металла — основного действующего начала в реакциях подавления детонации в результате взаимодействия металла с активными промежуточными продуктами. Начальным продуктом взаимодействия алкильных радикалов с кислородом обычно являются перекисный радикал ROO превращения которого приводят к образованию гидроперекисей, альдегидов и других соединений. Поскольку предплазменные превращения развиваются по цепному механизму, то на ранних стадиях процесса даже небольшое количество активного металла будет действовать эффективно, обрывая цепь в одном из ее звеньев, например, по схеме:
Этим обусловлена высокая эффективность малых добавок антидетонатора и постепенное ее снижение по мере увеличения содержания в горючем антидетонатора.
Металл образует низший окисел, способный далее окисляться до высших окислов за счет промежуточных продуктов или за счет кислорода воздуха. Активные промежуточные продукты превращаются в значительно более стабильные и менее реакционноспособные кислородные соединения – спирты или карбонильные производные.
Известны и другие схемы, объясняющие механизмы действия антидетонаторов; например, широкое распространение получила теория, по которой металл окисляется:
а затем
и
Для горючего с высокой термической стабильностью диссоциация начинается при температуре значительно более высокой, чем порог термического разложения антидетонатора; образующийся атомарный металл успеет прореагировать с кислородом до начала образования активных продуктов. В таких условиях металл окисляется до высших окислов, которые затрудняют развитие дальнейшего окисления.
Бензины, отличающиеся углеводородным составом, обладают различной приемистостью, т. е. при добавлении одного и того же количества антидетонатора детонационная стойкость их повышается не в одинаковой степени. Приемистость к антидетонатору зависит от соответствия температур термического разложения антидетонатора и интенсивного образования активных продуктов при окислении топлива. Например, порог начала термического разложения тетраэтилсвинца (ТЭС) равен приблизительно 200 °C:
Поэтому чем выше термическая стабильность углеводородов, тем менее эффективно будет действовать тераэтилсвинец. По отношению к некоторым углеводородам ТЭС проявляет нулевой и даже отрицательный антидетонационный эффект.
Тетраметилсвинец разлагается при температурах более высоких, чем тетрапропилсвинец. Поэтому для более термически стабильных углеводородов при большой степени сжатия ТМС эффективнее, чем ТЭС, а для бензинов с низкой детонационной стойкостью лучше тетрапропилсвинец. Существенным недостатком свинцовых антидетонаторов является их высокая токсичность.
Приемистость зависит также от содержания в бензине соединений, с которыми антидетонатор может взаимодействовать. При этом концентрация антидетонатора будет снижаться. Например, приемистость к ТЭС зависит от присутствия в бензине сернистых, галоидных и фосфорных соединений. В зависимости от вида этих соединений эффективность ТЭС снижается в разной степени.
Действие свинцовых антидетонаторов может усиливаться в присутствии некоторых веществ. Так, действие ТЭС усиливают (промотируют) органические кислоты и сложные эфиры.
Антидетонаторы на основе марганца и железа, несмотря на их довольно высокую эффективность и малую токсичность, не могут быть использованы, пока не будут найдены выносители окислов металла.
Вследствие высокой температуры плавления окислы металла, входящего в состав антидетонатора, не выносятся полностью с выпускными газами, а осаждаются на стенках камеры сгорания и цилиндра, на клапанах и свечах. Отложения в очень короткий срок выводят двигатель из строя. Поэтому антидетонаторы на основе металлов добавляются в бензины с веществами, способными при сгорании образовывать с металлом летучие соединения, более полно удаляющие их с выпускными газами.
Выносители не должны связывать металл очень рано или очень поздно. В первом случае эффективность действия антидетонатора будет снижена, а во втором – будут большие отложения в двигателе. Чем ниже температура плавления и выше давление паров образующегося соединения металла с элементами выносителя, тем полнее будет вынос металла и его окислов.
Выноситель и антидетонатор не должны значительно различаться по температуре кипения. Это необходимо для более равномерного распределения их в жидкой пленке по цилиндрам. Для свинца и его окислов найдены эффективные выносители. Это органические галоидные соединения (табл. 3).
| Таблица 3. Физические свойства выносителей для свинцовых антидетонаторов | |||||
|---|---|---|---|---|---|
| Характеристика | Дихлорэтан | Бромистый этил | Дибромэтан | Дибромпропан | α-монохлор-нафталин |
| Формула | C2H4Cl2 | C2H5Br | C2H4Br2 | C3H6Br2 | C10HCl7 |
| Плотность при 20 °C, г/см3 | – | 1,431 | 2,180 | 1,933 | 1,194 |
| Температура, °C: кипения плавления | – -35,3 | 38 -118 | 132 +10 | 142 -56 | 259 -20 |
| Давление насыщенных паров при 20 °C, мм рт. ст. | – | 399 | 10 | 6 | 1 |
Галоидные соединения жирного ряда эффективнее галоидопроизводных ароматического ряда. Из галоидных соединений жирного ряда бромсодержащие лучше, чем хлорпроизводные.
Механизм действия выносителей можно представить схемой: термическое разложение выносителя с образованием галоидоводорода или галоида и непредельного углеводорода:
Взаимодействие галоидоводорода или галоида с продуктами распада ТЭС и окислами свинца:
Смесь ТЭС, выносителя и наполнителя называется этиловой жидкостью.
Наиболее распространенной является жидкость Р9, в состав которой входит не менее 54 % ТЭС, 33 % бромистого этила и 6-7 % α-хлорнафталеина. Добавка этиловой жидкости, в бензин повышает его токсичность. Во избежание несчастных случаев, связанных с употреблением этилованных бензинов не по назначению, их окрашивают. При хранении ТЭС может разлагаться и окисляться, поэтому в состав этиловой жидкости вводят антиокислитель.
Присадки, улучшающие воспламеняемость дизельных топлив. В качестве присадок, ускоряющих процесс предпламенных превращений и тем самым облегчающих воспламенение, испытаны:
- алкилнитраты RCH2ONO2,
- алкилнитриты RCH2ONO,
- перекисные соединения RCH2OOH,
- альдегиды R CHO,
- кетоны RCOR и др.
Наиболее полно исследованы нитраты:
- Этил-,
- изо-пропил-,
- амил-,
- изо-амил- и циклогексилнитрат.
Подробно изучены азотнокислые эфиры циклопентанола и циклогексанола.
Добавки нитратов испытывались также с целью использования бензинов в дизелях. Особенно эффективен оказался циклогексилнитрат, добавка которого в количестве 1,2-1,5 % к этилированному бензину позволяла использовать его как топливо в быстроходных дизелях.
В процессах взаимодействия присадки с исходными углеводородами и их термического разложения образуются активные продукты, ускоряющие процессы предпламенных превращений, в результате чего сокращается период задержки воспламенения.
Оптимальное количество присадок составляет 1-3 %. Химический состав топлива не оказывает существенного влияния на эффективность их действия, хотя топлива ароматического основания менее восприимчивы к присадкам, чем алканового основания (табл. 4).
| Таблица 4. Повышение цетанового числа Цетановое число характеризует воспламеняемость дизельного топлива.x дизельного топлива при добавлении 2 % присадки | ||
|---|---|---|
| Присадка | Топливо прямой перегонки | Крекинг-гайзоль |
| Перекись ацетона | 19-24 | 18-22 |
| Этилнитрат | 18-21 | 16-20 |
| Изоамилнитрат | 18-22 | 16-22 |
С увеличением концентрации присадки ее относительная эффективность снижается.
Для повышения Применение горючих газов в качестве топлива в дизельных двигателяхцетанового числа дизельного топлива на 15-20 единиц необходимо добавлять не менее 1,5-2,0 % присадки. Присадки снижают стабильность топлива при хранении, при этом цетановое число топлива уменьшается. Большей устойчивостью обладают азотнокислые эфиры циклопентанола и циклогексанола.
Чем выше химическая стабильность топлива, чем устойчивее и действие присадок. В стабильном дизельном топливе прямой перегонки с добавкой нитроалканов цетановое число за шесть месяцев хранения снижается на один-два пункта.
Присадки для повышения полноты сгорания. Повышение полноты сгорания особенно важно в связи с необходимостью оздоровления окружающей среды. Неполное сгорание тяжелых топлив приводит к увеличению отложений в двигателе, при этом резко снижается долговечность и возрастает количество отказов в работе.
Протнвонагарные присадки к дизельным топливам на основе нафтенатов бария, меди и магния не получили широкого распространения, хотя они довольно значительно повышают полноту сгорания. Присадки, содержащие металлы, дают отложения, а беззольные присадки на основе азотных соединений оказались недостаточно эффективными.
Моющие беззольные присадки, обладающие поверхностно-активным действием (некоторые смолистые вещества, полимерные продукты и азотсодержащие соединения), в сочетании с нитратами (циклогексилнитрат и др.) повышают полноту сгорания и уменьшают образование отложений в дизеле.
Металлосодержащие присадки, растворимые в топливе, например нафтенаты и сульфонаты меди, магния и цинка, хелатные соединения и др., целесообразно использовать для тяжелых остаточных топлив. Такие присадки помимо растворимых соединений меди, магния и цинка обычно содержат ароматические соединения, растворяющие асфальтены и смолы. Для улучшения качества распыливания могут добавляться мыла на бариевой и кальциевой основе, снижающие поверхностное натяжение.
В результате лучшего распыливания и каталитического действия на процессы горения окислов меди и цинка достигается повышение полноты сгорания.
Для тяжелых топлив важно не только снизить количество отложений, но и изменить их характер. В отложениях присутствуют минеральные вещества, вызывающие коррозию. В золе остаточных топлив встречаются:
- ванадий,
- натрий,
- железо,
- никель,
- кальций и кремний.
Особенно опасны ванадий и натрий. Механизм коррозионного действия ванадия связан с его способностью проявлять переменную валентность и образовывать комплексные соединения, имеющие низкую температуру плавления.
Присадки переводят такие соединения, являющиеся переносчиками кислорода, в высокоплавкие продукты.
