Все виды судов, находясь в воде, подвергаются коррозии. Коррозия корпуса судна происходит на фоне агрессивности разных вод, которые незамедлительно влияют на металл и его физическое состояние. Наиболее агрессивной коррозионной средой является морская вода. При эксплуатации в морских условиях реализуются все известные типы коррозионных процессов. В табл. 1 приведены характеристики морской среды и их влияния на коррозию стали.
Высокая концентрация хлорид-ионов обусловливает питтинговую и язвенную коррозию нержавеющих сталей и алюминиевых сплавов. Действие морской воды приводит к снижению коррозионно-механической прочности конструкционных сталей, особенно при наличии в воде сероводорода.
Для высокопрочных алюминиевых сплавов опасными видами коррозии являются:
- контактная;
- щелевая;
- расслаивающая;
- язвенная;
- и коррозионное растрескивание.
При попадании морской воды или брызг на поверхность горячего оборудования (горячие трубопроводы, лопатки компрессоров, турбин и др.) возможна коррозия под пленкой при наличии высококонцентрированных растворов солей, приводящая к коррозионному растрескиванию и выходу из строя отдельных деталей.
В морских условиях основным видом коррозии является электрохимическая, так как морская вода — хороший электролит. Поверхность металла неоднородна: на ней существуют остатки окалины, ржавчины, поры и трещины.
В присутствии электролита создаются благоприятные условия для протекания электрохимической коррозии. На катодных участках образуются гидроксид-ионы, обладающие щелочными свойствами, а боковые стенки и дно язвенного углубления образуют анод, где металл растворяется, увеличивая размер язвы (рис. 1).
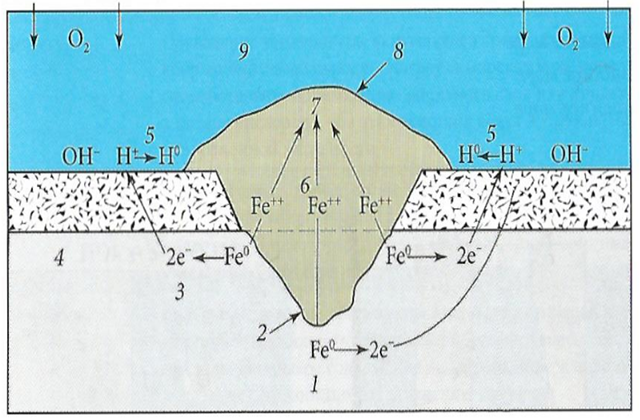
1 — анод (сталь); 2 — язва, образовавшаяся в результате разрушения железа; 3 — электроны; 4 — катод (окалина); 5 — ионы водорода; 6 — ионы железа; 7 — оксиды железа, пропитанные водой, содержащей кислород; 8 — плотный постепенно увеличивающийся в размерах бугорок ржавчины; 9 — вода, содержащая растворенный кислород
Интенсивность процесса находится в прямой зависимости от размеров катода, который при этом не изменяется, что показано на рис. 2.

а — характер разрушения анода; б — в морской воде при наличии электронов кислород способствует образованию на катоде щелочной зоны
Основные факторы, определяющие коррозионный процесс, приведены в табл. 2.
Определяющими факторами являются тип и количества растворенных солей, растворенного в воде кислорода, температура и скорость движения воды.
Эти факторы изменяются в зависимости прежде всего от местонахождения судна.
Растворенные соли
Соленость воды (суммарное содержание солей) выражают в промиллях (‰) — граммах веществ, содержащихся в 1 кг морской воды. Воды Атлантического и Тихого океанов содержат примерно 35 ‰ растворенных солей. Это количество различно в зависимости от региона и времени года. Так, в Красном море содержание солей в 2 раза больше, чем в Северном море. Максимальное содержание соли отмечается вблизи от берега.
Сравнительные данные по содержанию солей в водах разных морей и океанов приведены ниже:
Приблизительный состав солей в морской воде приведен в табл. 3
pH морской воды составляет 7,8-8,2. Удельная проводимость морской воды в арктической области равна 35 Ом·см, в Северном море — 24, а в тропических морях — 16.
Сильная агрессивность морской воды по сравнению с речной объясняется прежде всего высоким содержанием хлоридов. Ионы хлора не только повышают общую коррозионную активность, но и препятствуют образованию поверхностных или защитных покрытий или наносят вред уже существующим покрытиям. При местном снижении pH в результате гидролиза появляется коррозионный продукт, который играет роль анодной области, например под наслоениями или в щелях.
Читайте также: Ремонт подводной части судов
Для более активных материалов, например нелегированных или низколегированных сталей, это приводит к возникновению щелевой коррозии; для пассивных материалов, таких, как высоколегированные нержавеющие стали или алюминий и его сплавы, появляется «дырчатая» или «трещинная» коррозия. При повышенном содержании хлоридов для этих материалов увеличивается опасность образования стабильной дырчатой коррозии.
Содержание кислорода в воде
При Особенности коррозии в морской и пресной водекоррозии металла в морской воде происходит процесс восстановления воды растворенным кислородом:
Скорость этой реакции определяется скоростью диффузии кислорода к поверхности. При свободной поверхности скорость коррозии прямо пропорциональна концентрации кислорода в воде, хотя в определенной степени зависит от вида и концентрации растворенных солей. Содержание кислорода в морской воде зависит от температуры и при минус 10 °С составляет 0,5-0,6 ммоль/л и не зависит от глубины воды. На рис. 3 показано влияние содержания кислорода в воде на скорость коррозии нелегированной стали.
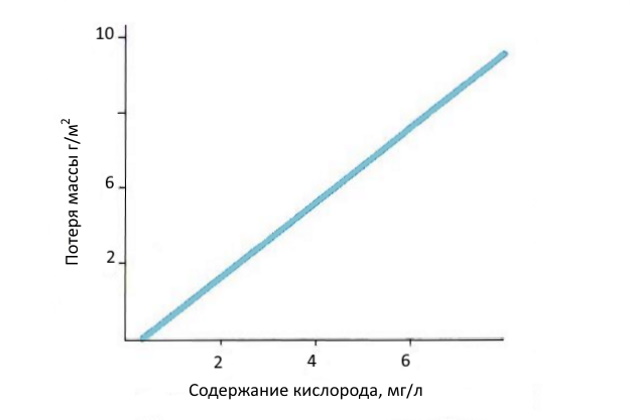
Недостаток кислорода в морской воде приводит к возникновению опасной щелевой коррозии, которая наблюдается в зоне «плеска» или при погружении судна. Металлы нуждаются в большом количестве кислорода для постоянного восстановления оксидной пленки, что обеспечивает пассивность в отношении щелевой коррозии, а также в морской воде. Этому виду коррозии обычно особенно подвержены нержавеющие стали и алюминиевые сплавы.
Если объект находится в стоячей морской воде и кислород расходуется на пломбирование вновь образующихся трещин в пассивирующей пленке с большей скоростью, чем поступает свежий кислород благодаря диффузии, то тенденция к щелевой коррозии возрастает (рис. 4).

Внешняя поверхность щели в контакте с несущей кислород морской водой действует как катод, а анодом является область под щелью, нижняя часть, которая по площади меньше катода и очень быстро разрушается. Такое начавшееся разрушение трудно остановить, так как для этого необходимо уменьшить внешнюю катодную область щели, например с помощью катодной защиты.
Щелевая коррозия появляется из-за наличия на поверхности металла шайб, заклепок, прокладок; причиной также могут быть осаждающиеся морские организмы типа ракообразных (barnacles) или моллюсков.
Наряду со щелевой наблюдается питтинговая коррозия, вызванная локальными дефектами на поверхности металла, которые могут возникать в процессе металлургического производства: включениями, разрывами в защитной пленке, усадкой металла и др. Основными факторами, влияющими на этот вид коррозии, являются малоподвижные условия, присутствие ионов тяжелых металлов (например, меди на алюминиевой поверхности), локальные включения инородных веществ. В этом случае питтинговая и щелевая коррозия протекают подобным образом.
Температура
Процесс коррозионного разрушения, как все химические реакции, зависит от температуры. Кроме того, температура влияет на содержание кислорода в воде.
Ниже приведены экспериментальные данные по определению содержания кислорода при различной температуре воды:
Из приведенных данных видно, что, например, для низколегированных сталей коррозионный процесс в теплых водах идет медленнее, чем в арктической зоне, из-за более низкого содержания кислорода в воде. На рис. 5 показано влияние скорости течения воды на протекание коррозии.
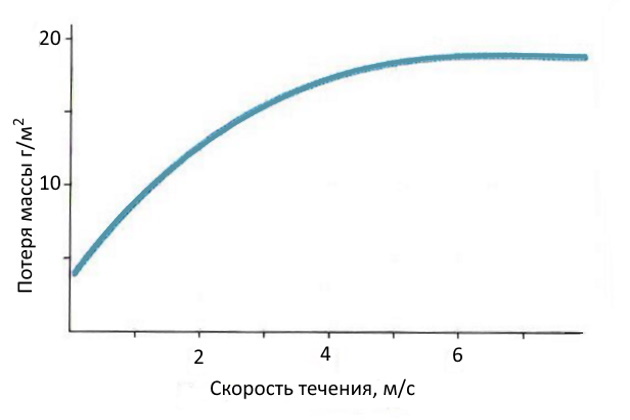
Рассматривая влияние различных факторов на коррозионные процессы, протекающие на корпусе суднаМатериалы по уходу за корпусом, следует отметить негативное действие осадков разной природы на поверхности судна, количество которых увеличивается в прибрежной полосе: бактерий, водорослей, морских червей, ракообразных и других морских организмов, описанных в статье “Обрастание судов различными микроорганизмами”Особенности обрастания водорослями и моллюсками корпусов судов. Эти осадки могут вызывать процессы коррозии из-за повреждения покрытий, на которых они образуются, а в ряде случаев могут также содействовать коррозионному процессу, как это делают сульфатвосстанавливающие бактерии. Все эти процессы относят к биологической коррозии, которая, как правило, существенных разрушений не производит, но обычно совмещается с другими видами коррозии.
Коррозионные процессы на поверхности корпуса судна происходят, естественно, не равномерно, а на разных участках с различной интенсивностью. Основной причиной этого является неоднородность металлов. В судовых условиях роль электродов выполняют стальной корпус и бронзовые втулки в дейдвудной трубе и рулевых петлях, а также бронзовый или латунный гребной винт. Медь и ее сплавы, обладая более высоким потенциалом, при контакте со сталью создают катод.
Будет интересно: Классификация современных кораблей, судов и их устройство
В результате этого сталь, являющаяся анодом, подвергается значительному коррозионному разрушению, особенно на участках, близко расположенных к местам контакта с катодом. При отсутствии разнородных металлов гальванические пары образуют сталь с окалиной и другими примесями и включениями. В некоторых случаях коррозия сосредоточивается на очень малой поверхности, вызывая глубокие разрушения в виде язв или точек. При очень сильном локальном воздействии коррозионного процесса возникает «дырчатая» коррозия, внешний вид которой показан на рис. 6.
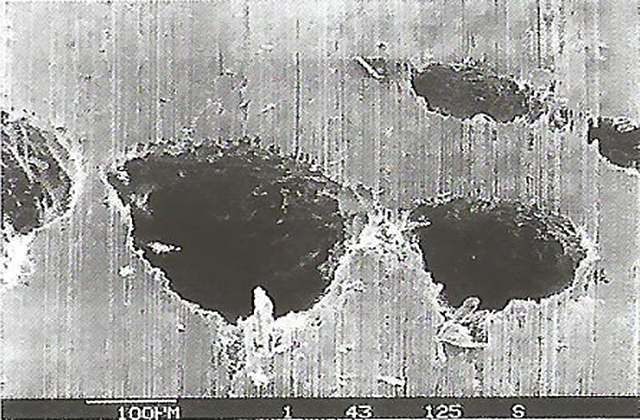
Наличие зазоров и щелей в металлической конструкции усиливает коррозию в морской воде.
Металл в щелях плохо аэрирован и играет роль анода, в связи с чем происходит его усиленное растворение. То же происходит на участках, не очищенных от прокатной окалины: окалина выступает в качестве катода, а чистый металл — в качестве анода. Аналогичный процесс наблюдается при наличии окрашенных и неокрашенных участков, а также при нарушении сплошности покрытия.
Процесс морской коррозии проходит по смешанному диффузионнокинетическому катодному механизму. При быстром движении морского судна или быстром течении может преобладать кинетический характер. При отсутствии движения преобладает диффузионный катодный механизм.
Коррозия наружных конструкций судна обусловлена действием морской воды — электролита на подводную часть корпуса, область переменной ватерлинии, надводный борт, палубы, надстройки, рубки, механизмы и оборудование, расположенные на палубах, куда попадает морская вода. Во внутренних помещениях коррозия возникает вследствие воздействия воздуха, насыщенного мелкими частицами воды, содержащей соли и растворенные газы. Коррозия сухогрузных трюмов является результатом действия морской воды или остатков перевозимых грузов, особенно если они гигроскопичны.
При электрохимической коррозии более чем при других ее видах происходят наибольшие разрушения металла корпуса, трубопроводов и другого судового оборудования. В результате коррозионного разрушения металл корпуса судна утоньшается, из-за чего снижается прочность отдельных конструкций и корпуса в целом. Следует учесть, что большинство деталей судовых механизмов и элементов корпуса подвергается одновременному воздействию механических напряжений и коррозионного разрушения.
Различают несколько видов коррозионномеханических разрушений:
- коррозионно-усталостное разрушение под действием переменных механических напряжений и коррозионной среды;
- коррозионное растрескивание под воздействием постоянных механических напряжений и коррозионной среды;
- коррозионно-кавитационные разрушения под воздействием пульсирующих механических напряжений и коррозионной среды.
На практике наиболее часто встречаются коррозионно-усталостные разрушения, которые могут привести к появлению трещин и постепенному их распространению в глубину металла перпендикулярно действию напряжений.
Участки судна испытывают действие различных агрессивных сред:
- морской воды,
- морской атмосферы,
- нефтепродуктов,
- конденсата и др., которые способствуют протеканию коррозионных процессов.
Характер и интенсивность разрушения зависят от многих факторов: района плавания, скорости хода, длительности рейса и эффективности защиты от коррозии. Электрохимическая коррозия приводит к разрушению сварных швов и металла около них из-за уже упомянутой разности потенциалов между материалом шва и основным материалом. Если металл шва имеет более отрицательный потенциал, чем основной материал, то сварной шов сильно разрушается. Если его потенциал более положительный, то разрушается не шов, а металл в окружающей области.
Предлагается к прочтению: Испытание корпуса судна на непроницаемость и герметичность
Из-за коррозионных разрушений морских судов возникают значительные потери металла, что требует больших материальных затрат на ликвидацию этих разрушений, а также на ремонт и замену оборудования, которое преждевременно выходит из строя или простаивает при разрушении отдельных деталей. Все это делает чрезвычайно актуальной задачу борьбы с морской коррозией.
Борьба с коррозией осуществляется различными методами, основными из которых являются:
- легирование;
- ингибиторная защита;
- электрохимическая защита;
- применение защитных покрытий.
Легирование не нашло широкого распространения в судостроении. Для повышения коррозионной стойкости сталей в качестве легирующих добавок применяют хром, никель, молибден, титан и другие металлы. Но достаточная эффективность их в морской воде обеспечивается только при содержании в стали легирующих элементов более 18%, что очень повышает ее стоимость. Поэтому из нержавеющей стали изготавливают только винты и подводные крылья.
Ингибиторную защиту применяют только в закрытых помещениях, например на нефтеналивных судах для предупреждения коррозии внутренней поверхности грузовых танков. Ингибитор вводится как в нефтепродукты, так и в принимаемую балластную воду в количестве сотых долей процента.
Электрохимическая защита может быть протекторной анодной или катодной. Протекторная защита состоит в присоединении к защищаемой конструкции пластины металла с более низким электродным потенциалом. Эта пластина-протектор становится анодом, на котором искусственно сосредоточивается коррозия. При разрушении протектора или потере его контакта с защищаемым материалом его заменяют новым.
Протекторы изготовляют из цинка, алюминия, магния и сплавов алюминия с цинком, магнием и другими металлами. Иногда в сплав вводят легирующие элементы: в протекторы из цинка — кадмий (0,025-0,15 %) или алюминий (0,1-0,5 %), в протекторы из алюминия — цинк (до 8 %) и магний (до 5 %), в протекторы из магния — алюминий (5-7 %) и цинк (2-5 %). Из них изготавливают бруски и закрепляют на корпусе судна (рис. 7). Наиболее эффективна протекторная защита в сочетании с лакокрасочными покрытиями.
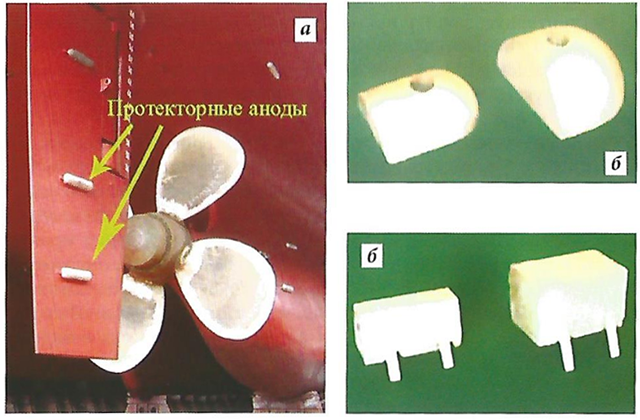
а — на корпусе судна; б — анодные протекторы
Второй вид защиты — защита внешним (наложенным) током — применяется для высоколегированных и высокохромированных сталей, олова, цинка, меди и их сплавов. Катодная защита основана на том, что при уменьшении потенциала металла можно снизить анодный ток до нуля или величины, при которой скорость коррозии не опасна для работы защищаемого сооружения. Это способ защиты принудительной катодной поляризацией с помощью внешнего источника постоянного тока. На рис. 8 показана схема системы катодной защиты внешним током подводной части корпуса судна.
Одна установка защищает конструкцию на протяжении большой длины, с ее помощью можно эффективно защищать объекты без применения специальных покрытий. Материал анода — это плакированная платиной медь, сплав серебра с 2 % свинца, хлорсеребряные электроды. Задачей установки является поляризация конструкции до равновесного потенциала железа в данном электролите.
Более простой способ защиты от коррозии — это нанесение защитных покрытий – лакокрасочных, металлических, неметаллических и оксидных. Наиболее широко в судостроении применяют лакокрасочные покрытия, которые наряду с невысокой стоимостью и простотой работ обеспечивают хорошую эффективность защиты от коррозии.
При защите металлических поверхностей от морской коррозии поверхность стали прежде всего тщательно очищают от прокатной окалины (пламенем, химическим травлением или пескоструйным методом). Затем наносят металлическое или лакокрасочное покрытие.
Металлические покрытия часто используют для защиты днища судов от морской коррозии. Самое распространенное из них — цинковое покрытие, толщина которого составляет 150-200 мкм. Его можно применять как самостоятельное защитное покрытие, а также в качестве основы под лакокрасочное покрытие. Для обивки днища морского судна с успехом используется легированный лантаном или цинком алюминий. Алюминиевое покрытие обладает высокой устойчивостью к коррозии и эрозии, его можно применять вместе с лакокрасочными покрытиями. Конструкции из сплавов алюминия защищают от морской коррозии с помощью оксидирования.
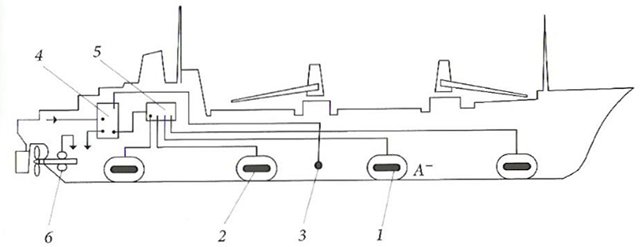
1 — аноды; 2 — околоанодный экран; 3 — электрод сравнения; 4 – источник питания; 5 — распределительный щит; 6 — контактно-щеточное устройство
При защите стали от морской коррозии поверхность сначала подвергают фосфатированию, а затем наносят толстослойное защитное лакокрасочное покрытие. Для защиты морских сооружений, эксплуатируемых в зоне периодического действия воды и ниже уровня воды на 1,5-2,0 м, рекомендуют применять систему покрытий, состоящую из слоя толщиной не менее 100 мкм, полученного термодиффузным цинкованием, и эпоксидного лакокрасочного покрытия толщиной не менее 150 мкм. Так как протекторные свойства покрытий ухудшаются с течением времени в связи с расходом цинка, то увеличение толщины позволит продлить их срок службы.
Для получения последующих защитных слоев лакокрасочных покрытий используются эпоксидные, виниловые, фенолформальдегидные, полиуретановые и другие пленкообразователи, при этом содержание растворителей должно быть минимальным. Особо устойчивыми к действию коррозионно-активных сред считаются фторполимерные покрытия.
Окраска судна осуществляется на судостроительной верфи. Применяемая система покрытий определяется характеристиками окружающей среды, в которой будет эксплуатироваться каждая часть судна.
Различается окраска поверхности на следующих участках судна:
- подводная часть;
- ватерлиния;
- надстройки в верхней части;
- внутренние площади и резервуары;
- верхние палубы;
- оборудование для подъема якоря.
Судостроительные заводы имеют отдельные помещения и участки для окрасочных работ. Система первичного покрытия, наносимого на стальные листы и детали, является «цеховой грунтовкой» для поддержания состояния конструкции во время строительства. Обычно она обогащена цинком или содержит в качестве пигмента силикат цинка.
Рекомендуется к прочтению: Натурные испытания судовых лакокрасочных покрытий для судов и кораблей
Окрасочные работы осуществляются на многих участках судостроительной верфи — от первоначального грунтования стали до окончательной окраски судна. Применяемые методы окраски различны и зависят от параметров конструкции и типа используемого ЛКМ. Окончательная окраска судна происходит на его борту, а отделочное покрытие выполняется на сборочном узле.

Пожалуйста скажите кто писал эту интересную статью и как сделать ссылку на нее?
Спасибо
Полезная информация, чтобы разбираться во всех этих деталях